
Wetenschap
Hoe gehoorzaamt zuurstof de Octect -regel bij het reageren om verbindingen te vormen?
De octetregel volgen:
* elektronische configuratie van Oxygen: Zuurstof heeft zes elektronen in de buitenste schaal (2S² 2P⁴). Om een stabiel octet te bereiken, moet het nog twee elektronen krijgen.
* Vorming van verbindingen: Zuurstof bereikt een stabiel octet door covalente bindingen te vormen met andere atomen en elektronen te delen. Bijvoorbeeld:
* water (h₂o): Zuurstof deelt twee elektronen met twee waterstofatomen, waardoor twee covalente bindingen worden gevormd. Dit geeft zuurstof in totaal acht elektronen in zijn valentieschil.
* koolstofdioxide (co₂): Zuurstof deelt twee elektronen met elk koolstofatoom en vormt twee dubbele bindingen. Dit resulteert opnieuw in acht elektronen rond zuurstof.
Uitzonderingen op de octetregel:
* HyperValent -verbindingen: In sommige verbindingen kan zuurstof meer dan acht elektronen in de valentieschaal hebben. Dit gebeurt in verbindingen zoals oxoniumion (h₃o⁺) , waarbij zuurstof drie covalente bindingen vormt en één eenzaam paar heeft. Het heeft in totaal tien elektronen in zijn valentieschil.
* vrije radicalen: Zuurstof kan bestaan als een vrije radicaal, zoals de superoxide -radicale (o₂⁻) . In dit geval heeft zuurstof zeven elektronen in zijn valentieschil.
Belangrijke punten om te onthouden:
* octetregel is een richtlijn: Het is een nuttig principe voor het begrijpen van binding, maar het is geen absolute regel.
* Uitzonderingen bestaan: Er zijn veel uitzonderingen op de octetregel, vooral met elementen in de tweede periode en daarna.
* Bonding begrijpen: Zelfs met uitzonderingen helpt de octetregel ons de drijvende kracht achter chemische binding en de stabiliteit van verbindingen te begrijpen.
Laat het me weten als je nog andere vragen hebt over zuurstof of de octetregel!
 NRL heeft patent verleend voor microbiële brandstofcel op zonne-energie
NRL heeft patent verleend voor microbiële brandstofcel op zonne-energie Welk type oplossing heeft meer waterstofionen?
Welk type oplossing heeft meer waterstofionen?  Wat is de algemene vergelijking voor dubbele verplaatsingsreactie?
Wat is de algemene vergelijking voor dubbele verplaatsingsreactie?  Scheidingstechniek van natriumchloride uit zijn oplossing in water?
Scheidingstechniek van natriumchloride uit zijn oplossing in water?  Wat is de opgeloste stof en het oplosmiddel in rozenwater?
Wat is de opgeloste stof en het oplosmiddel in rozenwater?
 Heeft de reisreactie van COVID-19 de deur geopend naar een nieuwe richting in het klimaatbeleid?
Heeft de reisreactie van COVID-19 de deur geopend naar een nieuwe richting in het klimaatbeleid? Non-profitorganisaties tonen veerkracht en initiatief tijdens het tweede jaar van de pandemie
Non-profitorganisaties tonen veerkracht en initiatief tijdens het tweede jaar van de pandemie  Pandemie:minder luchtvervuiling betekent dat er duizenden minder sterven
Pandemie:minder luchtvervuiling betekent dat er duizenden minder sterven Onderzoekers benadrukken het belang van regenwateronderzoek
Onderzoekers benadrukken het belang van regenwateronderzoek Waarom Mendel duizenden experiment op erwtenplanten?
Waarom Mendel duizenden experiment op erwtenplanten?
Hoofdlijnen
- Wat is moderne landbouw en traditionele landbouw?
- Wat voor soort voedsel wordt gemaakt zonder bacteriën?
- Wat is de relatie tussen structuur en functie van gespecialiseerde celstructuren?
- Welk voorbeeld beschrijft het beste een erfelijke eigenschap die kan worden bepaald door naar een individu te kijken?
- Wat zijn 4 manieren waarop micro -organismen het lichaam kunnen beschadigen?
- Hoe helpen decomposers de ecosysteemrecycle voedingsstoffen wanneer een boom sterft?
- Zullen we weten of TRAPPIST-1e leven heeft?
- Hoe wordt vertaling geïnitieerd in celbiologie?
- Wat is de wetenschappelijke in staat om te doen?
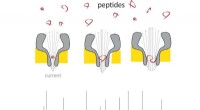
- Nanoporiën maken draagbare massaspectrometer voor peptiden werkelijkheid
- Van de bronstijd tot voedselblikken, hier is hoe tin de mensheid heeft veranderd

- Echografie kan sterkere 3D-geprinte legeringen maken

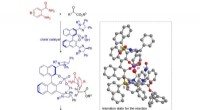
- Nieuwe methode voor asymmetrische N, N-acetaalsynthese belooft vooruitgang in de ontwikkeling van geneesmiddelen
- Brandstofcellen voor waterstofvoertuigen gaan langer mee

 Klimaatverandering en oceaanzuurstof:zuurstofarme zones zijn gekrompen tijdens warme perioden in het verleden, ontdekken wetenschappers
Klimaatverandering en oceaanzuurstof:zuurstofarme zones zijn gekrompen tijdens warme perioden in het verleden, ontdekken wetenschappers Is gedenatureerd en gehydrolyseerd eiwit hetzelfde?
Is gedenatureerd en gehydrolyseerd eiwit hetzelfde?  Wat is de betekenis van WR 104 in het bestuderen van dubbelstersystemen?
Wat is de betekenis van WR 104 in het bestuderen van dubbelstersystemen?  Easy Math Project Ideas
Easy Math Project Ideas Bij klimaatbesprekingen het is Amerika alleen meer dan Amerika eerst
Bij klimaatbesprekingen het is Amerika alleen meer dan Amerika eerst Hoe zorgen we ervoor dat leerlingen uit kansarme milieus vertrouwen krijgen in school?
Hoe zorgen we ervoor dat leerlingen uit kansarme milieus vertrouwen krijgen in school?  Generation Z-leden zeggen dat ze duurzame kleding willen, maar in plaats daarvan fast fashion kopen, zegt onderzoek
Generation Z-leden zeggen dat ze duurzame kleding willen, maar in plaats daarvan fast fashion kopen, zegt onderzoek Met welke uitdagingen staan mensen die in het berggebied wonen, worden geconfronteerd?
Met welke uitdagingen staan mensen die in het berggebied wonen, worden geconfronteerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

