
Wetenschap
Is fosfortrihydride -ionisch of covalent?
* Elektronegativiteitsverschil: Fosfor (P) en waterstof (H) hebben relatief vergelijkbare elektronegativiteitswaarden. Het verschil is niet groot genoeg om een significant ionisch karakter in de binding te creëren.
* delen van elektronen: In Ph₃ deelt Phosfor zijn elektronen met de drie waterstofatomen om covalente bindingen te vormen. Dit delen van elektronen resulteert in een stabiel molecuul.
Belangrijke opmerking: Hoewel de binding tussen fosfor en waterstof voornamelijk covalent is, heeft deze een kleine mate van polariteit vanwege het lichte elektronegativiteitsverschil. Dit betekent dat het fosforatoom een enigszins negatieve lading heeft en de waterstofatomen een enigszins positieve lading hebben.
 NASA ziet eerste tropische cycloon van het seizoen in de zuidelijke Stille Oceaan
NASA ziet eerste tropische cycloon van het seizoen in de zuidelijke Stille Oceaan Klauwen of niet klauwen? Het kattenvoorstel uit New York leidt tot een speels debat
Klauwen of niet klauwen? Het kattenvoorstel uit New York leidt tot een speels debat  Droogte en klimaatverandering waren de aanmaak, en nu staat de oostkust van Australië in vuur en vlam
Droogte en klimaatverandering waren de aanmaak, en nu staat de oostkust van Australië in vuur en vlam Wat verandert er als je de Antarctische Oceaan slechts 1 graad opwarmt? veel
Wat verandert er als je de Antarctische Oceaan slechts 1 graad opwarmt? veel Aardbeving in Zuidwest-China doet huizen instorten doodt minstens 3
Aardbeving in Zuidwest-China doet huizen instorten doodt minstens 3
Hoofdlijnen
- Het modelleren van antimicrobieel gebruik en resistentie in Canadese koppels kalkoenen
- Evolutie van binnenuit:onderzoek laat zien hoe virussen in darmbacteriën in de loop van de tijd veranderen
- Welke zou sneller mensen of bacteriën evolueren?
- Hoe je geur te verbergen voor honden
- Microscopische veerkenmerken onthullen de kleuren van fossiele vogels en verklaren waarom kasuarissen schitteren
- Hoe reproduceert een huisvlieg zich?
- Supercomputersimulatie onthult een nieuw mechanisme voor membraanfusie
- Kunnen alle levende wezens produceren?
- Waarom worden insectieve planten gedeeltelijke parasieten genoemd?
- Nieuwe katalysator geeft een boost aan de volgende generatie EV-batterijen
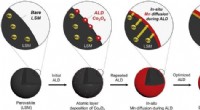
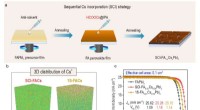
- Ontkoppeling van formamidinium–cesium perovskieten voor efficiënte fotovoltaïsche energie
- 3D-geprinte slimme gel verandert van vorm bij blootstelling aan licht

- Nieuwe gelcoatings kunnen leiden tot betere katheters en condooms

- Nieuwe tool om het ontdekken van medicijnen te versnellen
 De eerste chemicus die de wet van constante samenstelling formeel vermeldde, was?
De eerste chemicus die de wet van constante samenstelling formeel vermeldde, was?  Een tiltmeter is een vulkanisch monitoringtool dat meet?
Een tiltmeter is een vulkanisch monitoringtool dat meet?  Salpeterzuur plus natriumwaterstofcarbonaat?
Salpeterzuur plus natriumwaterstofcarbonaat?  Wat vogelsnavels zeggen over tropische biodiversiteit
Wat vogelsnavels zeggen over tropische biodiversiteit AI-kunst is nu overal. Zelfs experts weten niet wat het zal betekenen
AI-kunst is nu overal. Zelfs experts weten niet wat het zal betekenen Laserbursts wekken sneller elektriciteit op dan welke andere methode dan ook
Laserbursts wekken sneller elektriciteit op dan welke andere methode dan ook Uitgestorven stijl van platentektoniek verklaart de vroege platte bergen van de aarde
Uitgestorven stijl van platentektoniek verklaart de vroege platte bergen van de aarde Waar komt koolstofdioxide een plant binnen via STMOTA?
Waar komt koolstofdioxide een plant binnen via STMOTA?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

