
Wetenschap
Hoeveel elektronen zijn er in een zuurstofatoom wanneer het 2 Eltron -shell en 6 covalent atoom heeft?
* 2 elektronenschalen: Dit vertelt ons dat het zuurstofatoom elektronen heeft in zowel de eerste als de tweede energieniveaus.
* 6 covalente bindingen: Dit betekent dat het zuurstofatoom 6 elektronen deelt met andere atomen om covalente bindingen te vormen.
Hier is hoe we hierdoor kunnen redeneren:
* het atoomnummer van de zuurstof is 8: Dit betekent dat een neutraal zuurstofatoom normaal gesproken 8 elektronen heeft.
* Elektronenconfiguratie: De elektronenconfiguratie van Oxygen is 2, 6. Dit betekent dat 2 elektronen zich in de eerste schaal bevinden en 6 elektronen in de tweede schaal zijn.
* Covalente bindingen: Zuurstof vormt vaak 2 covalente bindingen (omdat het nog 2 elektronen nodig heeft om een stabiel octet te bereiken). Omdat het 6 elektronen in zijn tweede schaal heeft, deelt het 6 elektronen met andere atomen en vormt het 3 covalente bindingen in plaats van 2.
Daarom heeft het zuurstofatoom nog steeds 8 elektronen. Het heeft eenvoudig 6 van die elektronen gedeeld om 3 covalente bindingen met andere atomen te vormen.
 Om de zuurgraad van verschillende monsters theebladeren te bestuderen?
Om de zuurgraad van verschillende monsters theebladeren te bestuderen?  Infectie voorkomen met een verbeterde zilvercoating voor medische hulpmiddelen
Infectie voorkomen met een verbeterde zilvercoating voor medische hulpmiddelen Wie heeft een hogere elektronenaffiniteit tussen broom en jodium?
Wie heeft een hogere elektronenaffiniteit tussen broom en jodium?  Chemische reacties die kleurverandering veroorzaken
Chemische reacties die kleurverandering veroorzaken  Niet te nat, niet te droog - met plasma behandelde brandstofcel doet het precies goed
Niet te nat, niet te droog - met plasma behandelde brandstofcel doet het precies goed
 Neerslag in Deserts
Neerslag in Deserts Met plastic stro verbod, Washington keert zijn eigen uitvinding de rug toe
Met plastic stro verbod, Washington keert zijn eigen uitvinding de rug toe Mineralogie van de aardkorst drijft hotspots voor intraterrestrisch leven
Mineralogie van de aardkorst drijft hotspots voor intraterrestrisch leven COVID-19 en andere pandemieën zijn de effecten van onze negatieve impact op de diversiteit van het totale milieu
COVID-19 en andere pandemieën zijn de effecten van onze negatieve impact op de diversiteit van het totale milieu Wereldwijde database voor efficiënt watergebruik
Wereldwijde database voor efficiënt watergebruik
Hoofdlijnen
- Wetenschappers tonen positieve effecten aan van een beleid van positieve discriminatie ter bevordering van vrouwen
- Grootte is belangrijk:hoe lichaamsgrootte de verouderingspatronen van honden bepaalt
- Wat is extraverte eigenschap?
- Deze boom is het oudste levende organisme van Europa - een soort van,
- Onderzoekers breiden de kracht van genbewerking uit door een nieuwe klasse van DNA-basiseditors te ontwikkelen
- De oorsprong van het leven in een RNA-pocket
- Definieer wat een fysieke barrière is en eigenschappen van epitheel maken het een goede barrière?
- Wat is de opeenstapeling van verschillen tussen groepen die leiden tot de vorming van nieuwe soorten?
- Hoe peulvruchten zuurstof geven aan symbiotische bacteriën in hun wortels
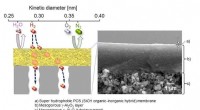
- Nieuw zuiveringsmembraan voor waterstofbrandstof maakt de weg vrij voor een groenere toekomst
- De hartslag kleuren
- Waarom een paar druppels water whisky beter laten smaken

- Geautomatiseerde chemie zet nieuw tempo voor materiaalontdekking

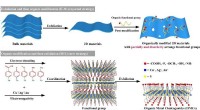
- 2-D geordende organische metaalchalcogeniden ontwikkeld met breed afstembare elektronische bandhiaten
 Burgers en wetenschappers publiceren 28-jarig record van waterkwaliteit in Buzzards Bay
Burgers en wetenschappers publiceren 28-jarig record van waterkwaliteit in Buzzards Bay Koolstofnanobuisjes kunnen de groei van celculturen die belangrijk zijn in de industrie verdubbelen
Koolstofnanobuisjes kunnen de groei van celculturen die belangrijk zijn in de industrie verdubbelen Het internet energiezuiniger maken door systemische optimalisatie
Het internet energiezuiniger maken door systemische optimalisatie Lichtgevoelige trigger ontwikkeld voor de geprogrammeerde celdeling en dood
Lichtgevoelige trigger ontwikkeld voor de geprogrammeerde celdeling en dood De oplosmiddelzeefmethode vestigt een nieuw record voor perovskiet lichtgevende dioden
De oplosmiddelzeefmethode vestigt een nieuw record voor perovskiet lichtgevende dioden  Wat zijn de algemene eigenschappen van overgangsmetalen?
Wat zijn de algemene eigenschappen van overgangsmetalen?  Onderzoeker ontdekt dat wanneer sperma concurreert, eieren hebben een keuze
Onderzoeker ontdekt dat wanneer sperma concurreert, eieren hebben een keuze Historische veranderingen in het Antarctisch ijs begrijpen, zou toekomstige veranderingen kunnen onthullen
Historische veranderingen in het Antarctisch ijs begrijpen, zou toekomstige veranderingen kunnen onthullen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

