
Wetenschap
Hoeveel zou het kookpunt van water toenemen als 4 mol NaCl werd toegevoegd aan 1 kg water (KB =0,51 ° C/(mol/kg) voor en i =2 NaCl)?
Hier leest u hoe u de kookpunthoogte kunt berekenen:
1. Bereken de molaliteit van de oplossing:
* Molaliteit (m) =mol opgeloste stof / kilogram oplosmiddel
* Molaliteit =4 mol NaCl / 1 kg H₂o =4 mol / kg
2. Bereken het kookpunthoogte (Δtb):
* Δtb =kb * i * m
* Δtb =0,51 ° C/(mol/kg) * 2 * 4 mol/kg =4,08 ° C
3. Bereken het nieuwe kookpunt:
* Het normale kookpunt van water is 100 ° C.
* Nieuw kookpunt =100 ° C + 4,08 ° C =104.08 ° C
Daarom zou het kookpunt van water met 4,08 ° C toenemen tot 104,08 ° C wanneer 4 mol NaCl wordt toegevoegd aan 1 kg water.
Hoofdlijnen
- Wat observeren wetenschapper het meest?
- De eerste gekweekte Chesapeake-zalm versus de laatste steur? Voorgestelde viskwekerij aan de oostkust wekt bezorgdheid op
- Hoe onderzoek ondersteunt de theorie?
- Hoe herhaalbaar is de evolutionaire geschiedenis?
- Wat is een fysieke beschrijving van amylase?
- Er is een microklimaat nodig om een pinyonboom te laten groeien
- Wat speelt een actieve rol in eiwitsynthese?
- Wat is de gecontroleerde variabele in experiment over spontane generatie?
- Het strandweer is hier en dat geldt ook voor haaien. Wetenschappers zeggen dat het tijd is om uit te kijken naar grote witte exemplaren
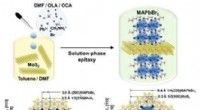
- Onconventioneel oplossingsproces voor 2-D heterostructuur
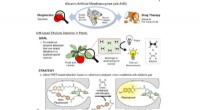
- Wetenschappers ontwikkelen metallo-enzym biosensor voor het monitoren van ethyleenniveaus in fruit
- Met een meerlagige aanpak, een filter om te voldoen aan de behoeften van de zoetwatervoorziening

- Water, bodemanalysetechnologie kan helpen bij het verbeteren van de sanering en monitoring op verontreinigde Superfund-locaties

- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

 Wat zijn de acht biomen van de aarde?
Wat zijn de acht biomen van de aarde?  De Skinwalker is niet zomaar een weerwolf
De Skinwalker is niet zomaar een weerwolf  Immuniteitspaspoorten kunnen helpen een einde te maken aan de lockdown, maar risicoklasse verdeelt en opzettelijke infecties
Immuniteitspaspoorten kunnen helpen een einde te maken aan de lockdown, maar risicoklasse verdeelt en opzettelijke infecties Consumer Electronics Show om internet-tv's te promoten
Consumer Electronics Show om internet-tv's te promoten  Hoe PPM in granen in waterhardheid te converteren
Hoe PPM in granen in waterhardheid te converteren Wat is de polariteit van natriumbenzoaat?
Wat is de polariteit van natriumbenzoaat?  Hoe Diodes in Circuit te testen
Hoe Diodes in Circuit te testen  Wetenschappers ontwikkelen een efficiëntere en economischere zonnecel op basis van grafeen en perovskiet
Wetenschappers ontwikkelen een efficiëntere en economischere zonnecel op basis van grafeen en perovskiet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


