
Wetenschap
Worden elementen meer metaalachtig geworden als je groepen doorgaat?
* toenemende atomaire straal: Naarmate je een groep naar beneden gaat, neemt het aantal elektronenschalen toe. Dit leidt tot een grotere atoomradius, wat betekent dat de buitenste elektronen verder weg van de kern zijn.
* Afnemende ionisatie -energie: De buitenste elektronen worden minder strak gehouden door de kern vanwege de verhoogde afstand. Dit resulteert in lagere ionisatie -energie, waardoor het gemakkelijker wordt om elektronen te verwijderen en positieve ionen te vormen, een belangrijk kenmerk van metalen.
* Afnemende elektronegativiteit: Elektronegativiteit, de neiging van een atoom om elektronen aan te trekken, neemt af naarmate je een groep doorgaat. Dit betekent dat de metalen in een groep minder kans hebben om elektronen aan te trekken en meer kans te verliezen, wat verder bijdraagt aan hun metalen karakter.
Uitzonderingen:
Hoewel de trend voor de meeste elementen geldt, zijn er enkele uitzonderingen, met name in de lagere groepen. Bijvoorbeeld:
* Groep 14: Tin (Sn) en lood (PB) vertonen een meer metaalachtig karakter in vergelijking met koolstof en silicium.
* Groep 15: Bismuth (BI) vertoont metalen eigenschappen ondanks dat ze zich in dezelfde groep bevinden als niet -metalen zoals stikstof en fosfor.
Onthoud: Het periodieke tabel is een prachtige weergave van trends, maar het is altijd belangrijk om individuele elementen en hun unieke eigenschappen te overwegen.
 Rechtbank steunt Californische vergoedingen voor vervuilers die limieten overschrijden
Rechtbank steunt Californische vergoedingen voor vervuilers die limieten overschrijden Onderzoeksteam neemt als eerste nieuwe equatoriale windpatronen waar op Antarctica
Onderzoeksteam neemt als eerste nieuwe equatoriale windpatronen waar op Antarctica Nieuw lab op een chip kan inspanningen voor koolstofopslag versnellen
Nieuw lab op een chip kan inspanningen voor koolstofopslag versnellen Mammoetjagers - weg met een gejammer of een knal?
Mammoetjagers - weg met een gejammer of een knal?  Opwarming in de stratosfeer leidt tot koude winters
Opwarming in de stratosfeer leidt tot koude winters
Hoofdlijnen
- Een gebied met een grote populatie waardevolle oceaanorganismen wordt een wat genoemd?
- Hoe de echidna zijn gif verloor
- Waarom beschouwen auteurs syndesmosis als een voorbeeld van amfiarthrose?
- Wat is malacologie?
- Habitats zijn veel kwetsbaarder voor stikstofdepositie dan eerder werd gedacht
- Waarom moeten chromosomen verdubbelen vóór mitose?
- Gaan we het nu echt over walvissen hebben?
- 'S Werelds botanische tuinen bevatten een derde van alle bekende plantensoorten, en help de meest bedreigde te beschermen
- Wat is een andere celnaam voor transplantaatafstotcellen?
- Kunstmatige zoetstof kan op een dag kankerbehandelingen bieden met minder bijwerkingen
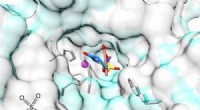
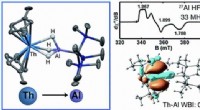
- Thorium-aluminiumcomplex het eerste met een actinide-element dat elektronen afstaat bij binding met een metaal
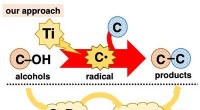
- Alcoholen als voorlopers van koolstofradicaal
- De groeiende mogelijkheden van biobased polymeren

- Een lasergestuurde programmeerbare contactloze transferdruktechniek

 Wat is de reikwijdte van de chemie in Pakistan?
Wat is de reikwijdte van de chemie in Pakistan?  Wetenschappers ontwikkelen Z-schema-katalysator voor verontreinigingen in water
Wetenschappers ontwikkelen Z-schema-katalysator voor verontreinigingen in water Industrieel gebruik voor kristallen
Industrieel gebruik voor kristallen Het meest complete portret van een supernova ooit
Het meest complete portret van een supernova ooit  Hoe zet je een scherpe atoomklok model spc 502 op?
Hoe zet je een scherpe atoomklok model spc 502 op?  Golven van verandering:Lagos in Nigeria bestrijdt Atlantische erosie
Golven van verandering:Lagos in Nigeria bestrijdt Atlantische erosie Hoe klimaatverandering emigratie uit Midden-Amerika stimuleert
Hoe klimaatverandering emigratie uit Midden-Amerika stimuleert Hoe vlammenwerpers werken
Hoe vlammenwerpers werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

