
Wetenschap
Wat is de maximale hoeveelheid elektronen die een atoom kan doneren en waarom?
* De elektronenconfiguratie van het atoom: Het aantal valentie -elektronen (elektronen in de buitenste schaal) bepaalt hoeveel elektronen een atoom gemakkelijk kunnen verliezen. Atomen met een kleiner aantal valentie -elektronen (zoals alkali -metalen met één valentie -elektron) hebben meestal meer kans om elektronen te doneren.
* De elektronegativiteit van het atoom: Elektronegativiteit is een maat voor de neiging van een atoom om elektronen aan te trekken. Atomen met lagere elektronegativiteit hebben meer kans om elektronen te doneren.
* De omliggende omgeving: Factoren zoals de aanwezigheid van andere atomen of moleculen kunnen de neiging van een atoom beïnvloeden om elektronen te doneren.
Dit is waarom er geen vast maximum is:
* ionisatie -energieën: Het verwijderen van elektronen uit een atoom vereist energie, ionisatie -energie genoemd. Elke opeenvolgende ionisatie vereist meer energie. Hoewel een atoom mogelijk meerdere elektronen kan verliezen, wordt het steeds moeilijker en energetisch ongunstig om meer elektronen te verwijderen.
* stabiliteit: Atomen hebben de neiging om elektronen te doneren om een stabiele elektronenconfiguratie te bereiken, die vaak op een edelgas lijken. Hoewel sommige atomen meerdere elektronen kunnen verliezen, verliezen ze niet meer dan nodig om deze stabiele toestand te bereiken.
Voorbeelden:
* Alkali -metalen (Li, Na, K, enz.): Ze doneren één elektron om kationen te worden met een +1 lading.
* alkalische aardmetalen (be, mg, ca, enz.): Ze kunnen twee elektronen doneren om kationen te vormen met een +2 lading.
* overgangsmetalen: Ze kunnen verschillende aantallen elektronen doneren, afhankelijk van het specifieke element en de voorwaarden, die vaak kationen vormen met meerdere mogelijke ladingen.
Samenvattend:
Een atoom kan een aantal elektronen doneren die worden bepaald door de specifieke elektronenconfiguratie, elektronegativiteit en de omliggende omgeving. Er is geen strikt maximum omdat het vermogen om elektronen te doneren afhankelijk is van de energievereisten en de stabiliteit van de resulterende ionen.
 Waar zijn kleine druppels vloeistoffen vloeistof van opgehangen in de lucht?
Waar zijn kleine druppels vloeistoffen vloeistof van opgehangen in de lucht?  Nieuwe connector voor duurzame constructies op aarde en in de ruimte
Nieuwe connector voor duurzame constructies op aarde en in de ruimte Oplossingen met pH lager dan 7 zijn?
Oplossingen met pH lager dan 7 zijn?  Wanneer een stof uitbreidt, wat gebeurt er met zijn massa?
Wanneer een stof uitbreidt, wat gebeurt er met zijn massa?  Onderzoekers kunnen nu snel nauwkeurig scannen op nutriëntengehalte in het gangpad met producten
Onderzoekers kunnen nu snel nauwkeurig scannen op nutriëntengehalte in het gangpad met producten
 Hittegolven bedreigen stadsbewoners, vooral minderheden en de armen
Hittegolven bedreigen stadsbewoners, vooral minderheden en de armen UITLEG:Fatale overstromingen in Pakistan hebben kenmerken van opwarming
UITLEG:Fatale overstromingen in Pakistan hebben kenmerken van opwarming Afvalwaterinjectiesnelheden zijn mogelijk de sleutel geweest tot de grootste aardbeving in Oklahoma's
Afvalwaterinjectiesnelheden zijn mogelijk de sleutel geweest tot de grootste aardbeving in Oklahoma's Waarom is fysieke geografie zo divers?
Waarom is fysieke geografie zo divers?  De mensheid heeft het ozongat genezen. Kunnen we hetzelfde doen voor klimaatverandering?
De mensheid heeft het ozongat genezen. Kunnen we hetzelfde doen voor klimaatverandering?
Hoofdlijnen
- Hoe fenotypische ratio te berekenen
- Welk voedsel bevat geen lipiden?
- Hoe laat de celtheorie zien dat de evolutie onjuist was?
- Wat maakt bruine rijst gezond? Het decoderen van de chemie van zijn voedingsrijkdom
- Hoe komt een kippenei aan zijn schaal?
- Welke structuren worden aangetroffen in dierlijke cellen, maar niet in plantencellen?
- Heerlijke eiwitballetjes:CSIRO maakt van rood vlees een voedzaam poeder
- Genen die verantwoordelijk zijn voor roodkleuring bij vogels gevonden
- Wetenschappers laten zien hoe aan botten grenzende cellen kunnen helpen bij het vormen van een schedel
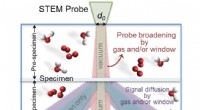
- Bepaling van de parameters voor transmissie-elektronenmicroscopie
- Ontdekking kan leiden tot duurzame ethanol gemaakt van koolstofdioxide

- Onderzoek wat titanium implantaten hun opmerkelijke biocompatibiliteit geeft

- UNT's moderne alchemist zet eerste stappen om methaan om te zetten in methanol
- Bij experimenten op aarde, mogelijke bouwstenen van buitenaards leven testen

 Voorbij lithium-ion:onderzoek naar de volgende generatie batterijen gaande
Voorbij lithium-ion:onderzoek naar de volgende generatie batterijen gaande Heb je je tas? De cruciale plaats van mobiele containers in de menselijke evolutie
Heb je je tas? De cruciale plaats van mobiele containers in de menselijke evolutie Het noordpoolgebied is meedogenloos; rijden in deze ijsbreker is niet
Het noordpoolgebied is meedogenloos; rijden in deze ijsbreker is niet Archeologische ontdekking levert aanwijzingen op over hoe onze voorouders hun omgeving mogelijk hebben aangepast
Archeologische ontdekking levert aanwijzingen op over hoe onze voorouders hun omgeving mogelijk hebben aangepast  Klimaatcrisis op een laag pitje nu pandemische dreiging opdoemt
Klimaatcrisis op een laag pitje nu pandemische dreiging opdoemt Review artikel bespreekt mogelijke rol, voordelen van niet-rhizobia-bacteriën in wortelknollen van peulvruchten
Review artikel bespreekt mogelijke rol, voordelen van niet-rhizobia-bacteriën in wortelknollen van peulvruchten Wat is het syntoisme van de kiemtheorie?
Wat is het syntoisme van de kiemtheorie?  Voordelen en nadelen van een frequentietabel
Voordelen en nadelen van een frequentietabel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

