
Wetenschap
Wat is de empirische formule voor een molecuul met 46,8 Si en 53.2 O?
Hier leest u hoe u de empirische formule kunt bepalen:
1. Ga uit van een 100 g monster:
* Dit maakt de berekeningen eenvoudiger. We hebben 46,8 g Si en 53,2 g O.
2. Converteer grams naar mollen:
* Verdeel de massa van elk element door zijn molaire massa:
* Si:46,8 g / 28,09 g / mol =1,66 mol
* O:53.2 g / 16.00 g / mol =3,33 mol
3. Vind de molverhouding:
* Verdeel elke molwaarde door de kleinste molwaarde (1,66 mol):
* Si:1.66 mol / 1.66 mol =1
* O:3,33 mol / 1.66 mol =2
4. Schrijf de empirische formule:
* De empirische formule is Sio₂ .
 Onderzoekers ontwikkelen molecuul dat kan leiden tot eerste synthetische antimalariamiddel in één dosis
Onderzoekers ontwikkelen molecuul dat kan leiden tot eerste synthetische antimalariamiddel in één dosis Wat heeft uranium te maken met ziekten?
Wat heeft uranium te maken met ziekten?  AI-systemen leren intuïtie te gebruiken om nieuwe medicijnen te vinden
AI-systemen leren intuïtie te gebruiken om nieuwe medicijnen te vinden  Wat is het verschil tussen kristal en kristallisatie?
Wat is het verschil tussen kristal en kristallisatie?  Wat is de standaardvorm van waterstof?
Wat is de standaardvorm van waterstof?
 De verschillen tussen mammoeten en olifanten
De verschillen tussen mammoeten en olifanten Wat is een wetenschappelijk woord voor feiten of cijfers?
Wat is een wetenschappelijk woord voor feiten of cijfers?  Nieuwe studie vindt verband tussen breukruwheid en de omvang van aardbevingen
Nieuwe studie vindt verband tussen breukruwheid en de omvang van aardbevingen Kenia verbiedt plastic voor eenmalig gebruik in beschermde gebieden
Kenia verbiedt plastic voor eenmalig gebruik in beschermde gebieden Flash droogte verergert in 14 zuidelijke staten van de VS
Flash droogte verergert in 14 zuidelijke staten van de VS
Hoofdlijnen
- Waarom verandert eiwit van kleur?
- Hoe kan het begrijpen van verkeerd gevouwen eiwitten de behandeling van ziekten helpen verbeteren?
- Bacteriën reproduceren meestal aseksueel, maar soms wisselen ze genetische informatie uit tijdens conjugatie Welke structuur vormen dit proces dat wordt gebruikt om info?
- Moleculaire biologie:zijn snel prolifererende cellen epigenetisch kneedbaar?
- Biomedical Engineering Project Onderwerpen voor High School
- Bacteriën hebben tastzin
- Waarom eten sommige bijenkoninginnen de eieren van hun werkbij?
- Hoe koeien tevreden te houden?
- 520 miljoen jaar oud wormfossiel lost het mysterie op van hoe moderne insecten, spinnen en krabben zijn geëvolueerd
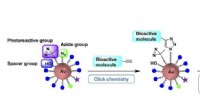
- Eenvoudig te monteren steigers van gouden nanodeeltjes dienen als moleculaire sonde
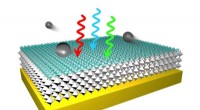
- Onderzoek kan de kosten van elektronenbronnen drastisch verlagen
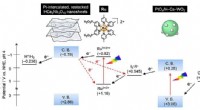
- Nieuwe fotokatalysator verhoogt de efficiëntie van watersplitsing voor schone waterstofproductie
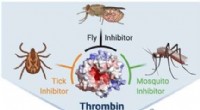
- Krachtige trivalente remmers van trombine uit antistollingspeptiden in speeksel van insecten
- Synthese van een zeldzaam metaalcomplex van lachgas opent nieuwe perspectieven voor
 ICE Cubes-ruimteonderzoeksdienst open voor bedrijven
ICE Cubes-ruimteonderzoeksdienst open voor bedrijven Waarom neemt het gewicht van een object af als het in een vloeistof wordt ondergedompeld. Wat is de relatiedichtheid in dit aspect?
Waarom neemt het gewicht van een object af als het in een vloeistof wordt ondergedompeld. Wat is de relatiedichtheid in dit aspect?  Convergentiewetenschap in het veranderende Noordpoolgebied
Convergentiewetenschap in het veranderende Noordpoolgebied  Ontdekking van oud glasvezelfossiel uit Glasgow onthult nieuwe soorten
Ontdekking van oud glasvezelfossiel uit Glasgow onthult nieuwe soorten  Naam van het zuur dat aanwezig is in chips?
Naam van het zuur dat aanwezig is in chips?  De mysteries van onderkoeld water verkennen
De mysteries van onderkoeld water verkennen Het coronavirus kan een revolutie teweegbrengen in het thuiswerken. Zijn we klaar?
Het coronavirus kan een revolutie teweegbrengen in het thuiswerken. Zijn we klaar? Akoestisch-optische modulatie van fotonische gebonden toestand in het continuüm
Akoestisch-optische modulatie van fotonische gebonden toestand in het continuüm
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

