
Wetenschap
Hoe zijn de verschillende secties van het periodieke tabel dat wordt genoemd?
1. Perioden:
- Horizontale rijen worden perioden genoemd .
- Er zijn 7 periodes In de periodiek systeem, genummerd 1 tot en met 7.
- Elementen binnen een periode hebben hetzelfde aantal elektronenschalen.
2. Groepen (of families):
- Verticale kolommen worden groepen genoemd of gezinnen .
- Er zijn 18 groepen In het periodiek systeem, genummerd 1 tot en met 18.
- Elementen binnen een groep hebben hetzelfde aantal valentie -elektronen (elektronen in de buitenste schaal) en delen vergelijkbare chemische eigenschappen.
3. Blokken:
- Het periodiek systeem is ook verdeeld in vier blokken Gebaseerd op de subshells die worden gevuld:
- S-blok: Groepen 1 en 2 (alkali en alkalische aardmetalen)
- P-block: Groepen 13 tot 18 (inclusief niet -metalen, halogenen en edelgassen)
- D-blok: Groepen 3 tot 12 (overgangsmetalen)
- F-blok: Lanthaniden en actiniden (binnenovergangsmetalen)
4. Andere classificaties:
- metalen: De meeste elementen zijn metalen. Ze zijn over het algemeen glanzend, kneedbaar, ductiele en goede geleiders van warmte en elektriciteit.
- Niet -metalen: Gelegen aan de rechterkant van het periodiek systeem, missen niet -metalen de eigenschappen van metalen.
- metalloïden: Deze elementen hebben eigenschappen die liggen tussen die van metalen en niet -metalen. Ze staan ook bekend als semimetalen.
- Representatieve elementen: Deze elementen bevinden zich in het S-blok en P-blok.
- Transitie -elementen: Deze elementen bevinden zich in het D-blok en hebben variabele oxidatietoestanden.
Inzicht in deze verschillende secties helpt u om de trends in eigenschappen in het periodiek systeem te begrijpen.
 Wat zijn de namen en formules voor oxyzuren jodium?
Wat zijn de namen en formules voor oxyzuren jodium?  Fruitige thiolen opsnuiven in hoppige bieren
Fruitige thiolen opsnuiven in hoppige bieren Materiaal voor veiligere voetbalhelmen kan hoofdletsel verminderen
Materiaal voor veiligere voetbalhelmen kan hoofdletsel verminderen Waar zijn de meeste elementen van gemaakt?
Waar zijn de meeste elementen van gemaakt?  Bij het meten van een kleine hoeveelheid vloeistof zou welk instrument de meest nauwkeurige lezing mogelijk maken?
Bij het meten van een kleine hoeveelheid vloeistof zou welk instrument de meest nauwkeurige lezing mogelijk maken?
 Verweringspercentages voor gedolven land exponentieel hoger dan niet-gemijnde sites
Verweringspercentages voor gedolven land exponentieel hoger dan niet-gemijnde sites Psychologen testen maatschappelijke acceptatie ondergrondse opslag CO2
Psychologen testen maatschappelijke acceptatie ondergrondse opslag CO2 Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen
Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen Duitsland plant klimaatactie ter waarde van meer dan 100 miljard euro
Duitsland plant klimaatactie ter waarde van meer dan 100 miljard euro Mariene cyanobacteriën overleven niet alleen op fotosynthese
Mariene cyanobacteriën overleven niet alleen op fotosynthese
Hoofdlijnen
- Rusland? China? Wie heeft Yahoo gehackt, en waarom?
- Ziek dolfijnkalf verbetert met sondemelk, helpende handen
- Gesynchroniseerd:hoe cellen verbindingen maken, kan van invloed zijn op het circadiane ritme
- Een nieuwe manier om metabolic engineering te doen
- Hoe een team van biologen een plaag aanpakt en soorten voor uitsterven behoedt
- Theory of Evolution: Definition, Charles Darwin, Evidence & Voorbeelden
- Herziening van historische voorraadroutes kan zeldzame stukken inheemse planten en dieren in gevaar brengen
- AI-aangedreven virtuele rat biedt inzicht in hoe hersenen complexe, gecoördineerde bewegingen controleren
- Onderzoek van moleculaire componenten die verantwoordelijk zijn voor het genereren van de actiepotentiaal in de Flytrap van Venus
- Onderzoeker creëert chemisch systeem dat vroeg celgedrag nabootst

- Ontwikkeling van een 3D-deeltjesmodel voor afzonderlijke deeltjes in batterij-elektroden
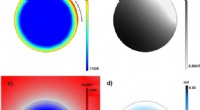
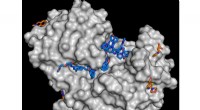
- Nieuwe stoffenbibliotheek om het zoeken naar actieve stoffen te versnellen
- Nieuwe melkzuurbacteriën zorgen voor natuurlijke zoetheid in yoghurt

- Titaniumkatalyse maakt stereoselectieve synthese van C-glycosiden en glycopeptiden mogelijk
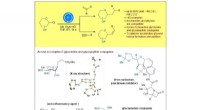
 Wat wordt gebruikt als een sjabloon voor replicatie?
Wat wordt gebruikt als een sjabloon voor replicatie?  Handel met voorkennis:nog een glazen plafond?
Handel met voorkennis:nog een glazen plafond?  Alternatief vlees gezien als potentieel sappige business
Alternatief vlees gezien als potentieel sappige business Wat zijn de 6 stappen van transcriptie?
Wat zijn de 6 stappen van transcriptie?  Een ontsmettingsmiddel in het galactische centrum
Een ontsmettingsmiddel in het galactische centrum De fysiologie van ondoordringbare huid:Colossus of the X-men
De fysiologie van ondoordringbare huid:Colossus of the X-men Spuiten waterpluimen uit Europa? NASA's Europa Clipper zit op de zaak
Spuiten waterpluimen uit Europa? NASA's Europa Clipper zit op de zaak Hoe Earth 911.org werkt
Hoe Earth 911.org werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

