
Wetenschap
Een binding tussen twee atomen met een verschil in elektronegativiteiten groter dan 1,7 wordt geclassificeerd als?
Dit is waarom:
* elektronegativiteit: Dit is een maat voor het vermogen van een atoom om elektronen naar zichzelf aan te trekken in een chemische binding.
* ionische bindingen: Vorm wanneer er een significant verschil is in elektronegativiteit tussen twee atomen. Het atoom met hogere elektronegativiteit zal een elektron "stelen" van het atoom met lagere elektronegativiteit, wat resulteert in de vorming van ionen (geladen deeltjes).
* Covalente bindingen: Vorm wanneer atomen elektronen delen. Deze bindingen treden meestal op wanneer het elektronegativiteitsverschil minder is dan 1,7.
Voorbeeld:
* Natrium (NA) heeft een lage elektronegativiteit, terwijl chloor (CL) een hoge elektronegativiteit heeft. Het verschil in elektronegativiteit is groot genoeg om een ionische binding te vormen, wat resulteert in de vorming van natriumchloride (NaCl) of tafelzout.
 Niets te eten behalve cactus in de hongerhoofdstad van Madagaskar
Niets te eten behalve cactus in de hongerhoofdstad van Madagaskar Hoe gaan we om met de vraag naar water nu we een tijdperk van schaarste ingaan?
Hoe gaan we om met de vraag naar water nu we een tijdperk van schaarste ingaan? Chinese koolstofmarkt legt Australische energieverlamming bloot
Chinese koolstofmarkt legt Australische energieverlamming bloot Hoe heet water dat in de grond dringt?
Hoe heet water dat in de grond dringt?  Isotopische samenstelling van atmosferisch sulfaat en nitraat
Isotopische samenstelling van atmosferisch sulfaat en nitraat
Hoofdlijnen
- Leuke wasberen zijn superleerlingen en waarschijnlijk criminele meesterbreinen uit de vuilnisbak
- De functies van cytoplasma in een cel?
- Het raadsel van de instandhouding:hoe kies je welke soort je wilt beschermen?
- Jesse keek naar een cel via microscoop en zag mitochondria membranen wat zou kunnen zeggen over de cel?
- Onderzoek laat zien hoe een enkel enzym de productie van sojaolie kan stimuleren
- Rudolph, waarom is je neus zo helder? Wetenschappers van Johns Hopkins hebben een idee
- Met welke geërfde eigenschappen worden mensen geboren?
- Wat is apoptose?
- Vergeet uw huisdieren niet tijdens koud weer
- Nieuw mechanisme voor het reguleren van de aanvoer van DNA-bouwstenen voor betere antibiotica
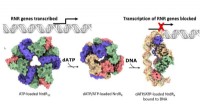
- Experiment verbetert voorspellingen van uraniumverspreiding

- Het naderen van een ideale aminozuursynthese met behulp van waterstof
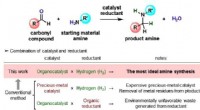
- Spiegels regelen de chemische selectiviteit

- Door het kijkglas:ontrafelen hoe ionen bewegen in fosfaatglas

 Baanbrekende wiskundige formule maakt de weg vrij voor spannende ontwikkelingen in de gezondheids-, energie- en voedingsindustrie
Baanbrekende wiskundige formule maakt de weg vrij voor spannende ontwikkelingen in de gezondheids-, energie- en voedingsindustrie Nanodeeltjes liften mee op immuuncellen om kankeruitzaaiingen vroegtijdig op te sporen
Nanodeeltjes liften mee op immuuncellen om kankeruitzaaiingen vroegtijdig op te sporen  Onjuiste breuken oplossen Math-problemen
Onjuiste breuken oplossen Math-problemen Hoe hoeken in driehoek te berekenen
Hoe hoeken in driehoek te berekenen  Het recht om zich los te maken van het werk – en toezicht op de werkgever – groeit wereldwijd. Waarom blijft NZ achter?
Het recht om zich los te maken van het werk – en toezicht op de werkgever – groeit wereldwijd. Waarom blijft NZ achter?  Hoe teleportatie zal werken
Hoe teleportatie zal werken  Hebben emoties invloed op beslissingen over straf in de context van misdaad?
Hebben emoties invloed op beslissingen over straf in de context van misdaad? Is helium een vaste vloeistof of gaskamer?
Is helium een vaste vloeistof of gaskamer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

