
Wetenschap
Hoe wordt de pH -schaal ingesteld?
1. Het bereik:
* De pH -schaal varieert van 0 tot 14.
* Een pH van 7 is neutraal , wat betekent dat de oplossing niet zuur noch alkalisch is.
* Oplossingen met een pH onder 7 zijn zuur , met lagere getallen die een sterkere zuurgraad aangeven.
* Oplossingen met een pH boven 7 zijn alkalisch (basic) , met hogere getallen die een sterkere alkaliteit aangeven.
2. De logaritmische aard:
* De pH -schaal is logaritmisch, wat betekent dat elke gehele getalverandering in pH een tienvoudige verandering in waterstofionconcentratie vertegenwoordigt ([H+]).
* Een oplossing met een pH van 5 heeft bijvoorbeeld tien keer de waterstofionconcentratie van een oplossing met een pH van 6.
3. De formule:
* De pH van een oplossing wordt berekend met behulp van de volgende formule:
pH =-log [H+]
Waar:
* pH is de pH van de oplossing
* [H+] is de concentratie waterstofionen in mol per liter (mol/L).
Samenvattend:
* De pH -schaal is een handige manier om de zuurgraad of alkaliteit van een oplossing uit te drukken.
* Een lagere pH duidt op een hogere zuurgraad, een hogere pH duidt op een hogere alkaliteit en een pH van 7 is neutraal.
* De schaal is logaritmisch, dus een verandering van één pH -eenheid vertegenwoordigt een tienvoudige verandering in waterstofionconcentratie.
Voorbeeld:
* Een oplossing met een pH van 3 is 100 keer zuurder dan een oplossing met een pH van 5.
* pH 3:[H+] =10^-3 mol/l
* pH 5:[H+] =10^-5 mol/l
 Nieuwe elektrochemische sensor detecteert gevaarlijke bacteriën
Nieuwe elektrochemische sensor detecteert gevaarlijke bacteriën  Instant messaging in eiwitten ontdekt
Instant messaging in eiwitten ontdekt Een beter duurzaam maandverband
Een beter duurzaam maandverband Chemici ontwikkelen een nieuwe methode om gefluoreerde componenten in moleculen te introduceren
Chemici ontwikkelen een nieuwe methode om gefluoreerde componenten in moleculen te introduceren  Wanneer het volume van gas wordt verdubbeld bij het doen van de atmosferische druk zal zijn?
Wanneer het volume van gas wordt verdubbeld bij het doen van de atmosferische druk zal zijn?
 Helft van wereldwijd gezuiverd afvalwater, tarieven in ontwikkelingslanden nog steeds achter
Helft van wereldwijd gezuiverd afvalwater, tarieven in ontwikkelingslanden nog steeds achter Wat is een voorbeeld van slib?
Wat is een voorbeeld van slib?  Nieuw systeem voor vroegtijdige waarschuwing kan kwetsbare eilanden beschermen tegen overstromingen
Nieuw systeem voor vroegtijdige waarschuwing kan kwetsbare eilanden beschermen tegen overstromingen NASA kijkt naar tropische cyclonen Irwin en Hilary regenval en Fujiwara-effect
NASA kijkt naar tropische cyclonen Irwin en Hilary regenval en Fujiwara-effect Aardbeving treft New Jersey, schudden gerapporteerd over de staat
Aardbeving treft New Jersey, schudden gerapporteerd over de staat
Hoofdlijnen
- Wat doet osmose met planten- en dierlijke cellen in zuiver water?
- Hoe klimaatverandering planten onder druk zet en hun groei verandert
- Universeel klemeiwit stabiliseert gevouwen eiwitten:nieuw inzicht in hoe de chaperonne Hsp70 werkt
- Welk deel van cellulaire ademhaling moet plaatsvinden voordat een andere stap kan optreden?
- Het verkennen van een oude gebeurtenis in pompoen, evolutie van kalebas en meloen
- Wat is het aantal kerncellen?
- Waarom je kat deze 6 dingen doet volgens de wetenschap
- Wat is de beste definitie van het woord pathogeen?
- Wat doodde tonnen vissen in de Europese rivier? Het mysterie wordt dieper
- Op zoek naar een uit-schakelaar voor coeliakie
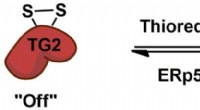
- Mechanische eigenschappen van viraal DNA bepalen het verloop van infectie

- Nieuwe manier om influenza A-virus te identificeren licht op wanneer specifieke virusdoelen aanwezig zijn
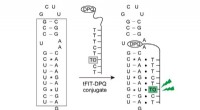
- Nieuw elektrodeontwerp kan leiden tot krachtigere batterijen
- methaanthiol, een potentiële nieuwe grondstof in de C1-chemie

 Chinese verstedelijking 2050 – systeem dynamische modellering en processimulatie
Chinese verstedelijking 2050 – systeem dynamische modellering en processimulatie Kan China de jaarlijkse vermindering van de vervuiling volhouden?
Kan China de jaarlijkse vermindering van de vervuiling volhouden?  Gelaagde kalksteenafzettingen geven een uniek inzicht in Romeinse aquaducten
Gelaagde kalksteenafzettingen geven een uniek inzicht in Romeinse aquaducten De betrouwbaarheid van het stroomsysteem beoordelen in een veranderend net, omgeving
De betrouwbaarheid van het stroomsysteem beoordelen in een veranderend net, omgeving Relikwieën uit Shakespeares huis gedeeld in nieuwe virtuele tentoonstelling
Relikwieën uit Shakespeares huis gedeeld in nieuwe virtuele tentoonstelling Wat is de zwaartekracht van de maan ten opzichte van die aarde?
Wat is de zwaartekracht van de maan ten opzichte van die aarde?  Noem een exoplaneet
Noem een exoplaneet Neanderthalers waren artistiek zoals moderne mensen, studie geeft aan:
Neanderthalers waren artistiek zoals moderne mensen, studie geeft aan:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

