
Wetenschap
Wat is de grootte van een mol in de chemie?
Een mol in chemie is geen maat, maar een hoeveelheid . Het is een eenheid die wordt gebruikt om de hoeveelheid van een stof te meten. Dit is wat het betekent:
* Eén mol is gelijk aan 6.022 x 10^23 deeltjes van een stof. Dit nummer staat bekend als het nummer van Avogadro.
* De deeltjes kunnen atomen, moleculen, ionen of een ander type elementaire entiteit zijn.
* De massa van één mol van een stof is gelijk aan het atoom- of molecuulgewicht tot expressie gebracht in gram. Een mol koolstofatomen weegt bijvoorbeeld 12,01 gram.
Denk er zo aan: Een dozijn betekent 12, een bruto betekent 144 en een mol betekent 6.022 x 10^23. Het is een handige manier om extreem grote aantallen kleine deeltjes te tellen.
 Doet acrylonitril butadieen styreen plastic dwz. ABS bevat bisfenol-a?
Doet acrylonitril butadieen styreen plastic dwz. ABS bevat bisfenol-a?  Is helium een liqiud of vast gas?
Is helium een liqiud of vast gas?  Hoe robotwiskunde en smartphones onderzoekers naar een doorbraak in de ontdekking van medicijnen hebben geleid
Hoe robotwiskunde en smartphones onderzoekers naar een doorbraak in de ontdekking van medicijnen hebben geleid Wat is de chemische vergelijking voor een niet-lichtgevende vlam?
Wat is de chemische vergelijking voor een niet-lichtgevende vlam?  Wat wordt er gebruikt in een atoombom?
Wat wordt er gebruikt in een atoombom?
Hoofdlijnen
- Wat is een organisme dat de groeisnelheid van het organisme kan beperken?
- Hoe produceren planten voedsel van fotosynthese?
- Is Magic Mushroom een natuurlijke vorm van zuur?
- Genexpressie in Prokaryotes
- Mottenvrouwtjes gebruiken geurnabijheid om partners aan te trekken
- Zit moraliteit in de hersenen?
- Duurzame zeevruchten bovenaan het menu voor nieuwe onderzoeksgroep
- Slapen wolven als honden?
- Hoe videogames de inspiratie vormden voor een strijd tegen mitochondriale ziekten
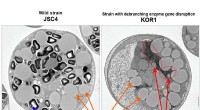
- Koolhydraten omzetten in lipiden voor biobrandstoffen voor microalgen
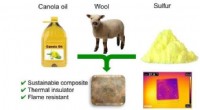
- Nieuwe isolatie haalt warmte uit de omgeving
- Computermodel kan wetenschappers helpen uit elkaar te gaan, eiwitten opnieuw samenstellen op commando

- Een nieuw materiaal om mechanisch robuuste en vormveranderende structuren te printen

- Superieure waterstofkatalysator groeit gewoon zo

 Hoeveel centimeter in 190 cm?
Hoeveel centimeter in 190 cm?  Manilla pakt het plasticprobleem aan via een door de gemeenschap geleid protocol
Manilla pakt het plasticprobleem aan via een door de gemeenschap geleid protocol  Rapport onthult seizoensgebonden ijzeruitputting in Britse kustwateren
Rapport onthult seizoensgebonden ijzeruitputting in Britse kustwateren Zeewier als biobrandstof? Metabolic engineering maakt het een haalbare optie
Zeewier als biobrandstof? Metabolic engineering maakt het een haalbare optie  Vraag en antwoord:Waarom verdrinken we in plastic voor eenmalig gebruik, en wat kunnen we eraan doen?
Vraag en antwoord:Waarom verdrinken we in plastic voor eenmalig gebruik, en wat kunnen we eraan doen?  Stijgende zeeën bedreigen laaggelegen kuststeden, 10% van de wereldbevolking
Stijgende zeeën bedreigen laaggelegen kuststeden, 10% van de wereldbevolking Waarom schijnt de zon?
Waarom schijnt de zon?  Natuurlijke stoffen zijn veelbelovend tegen het coronavirus
Natuurlijke stoffen zijn veelbelovend tegen het coronavirus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

