
Wetenschap
Welk volume waterstof in L wordt geproduceerd uit de volledige reactie van 3143 molkenzuur 3143 mol bij STP mg S 2HCl aq mgcl2 H2 g?
1. Evenwichtige chemische vergelijking:
De evenwichtige chemische vergelijking voor de reactie is:
Mg (s) + 2HCl (aq) → mgcl₂ (aq) + h₂ (g)
2. Mol -verhouding:
Uit de evenwichtige vergelijking zien we dat 2 mol HCl reageert om 1 mol H₂ te produceren.
3. Mol Mol H₂ geproduceerd:
Omdat we 3143 mol HC1 hebben, kunnen we de mol H₂ geproduceerd berekenen:
* (3143 mol HCl) * (1 mol H₂ / 2 mol HC1) =1571,5 mol H₂
4. Volume van H₂ op STP:
Bij standaardtemperatuur en druk (STP) bezet 1 mol ideaal gas 22,4 L. We kunnen dit gebruiken om het volume van de geproduceerde H₂ te berekenen:
* (1571,5 mol H₂) * (22.4 l/mol) = 35,213.6 l
Daarom worden 35,213,6 liter waterstofgas geproduceerd uit de volledige reactie van 3143 mol zoutzuur bij Stp.
 Hoe ondergaan de huishoudelijke schoonmaakmiddelen chemische veranderingen?
Hoe ondergaan de huishoudelijke schoonmaakmiddelen chemische veranderingen?  Hoe krijg je opgeloste stoffen uit water?
Hoe krijg je opgeloste stoffen uit water?  Met behulp van licht, rode bloedcellen en een honingbijpeptide om therapeutische eiwitten te leveren
Met behulp van licht, rode bloedcellen en een honingbijpeptide om therapeutische eiwitten te leveren Chemische vergelijking voor het verbranden van fossiele brandstoffen?
Chemische vergelijking voor het verbranden van fossiele brandstoffen?  Onderzoekers ontdekken hoe te veel zuurstof cellen en weefsels beschadigt
Onderzoekers ontdekken hoe te veel zuurstof cellen en weefsels beschadigt
 Huizen en hoogbouw (en niets ertussenin):waarom landzonering niet effectief is geweest voor het verbeteren van de stedelijke dichtheid
Huizen en hoogbouw (en niets ertussenin):waarom landzonering niet effectief is geweest voor het verbeteren van de stedelijke dichtheid  Noem de drie soorten obligaties, van minst aantrekkelijk tot meest aantrekkelijk?
Noem de drie soorten obligaties, van minst aantrekkelijk tot meest aantrekkelijk?  Sociologen debatteren over de vraag:zijn Amerikanen werkelijk geïsoleerd?
Sociologen debatteren over de vraag:zijn Amerikanen werkelijk geïsoleerd?  Toegangspoort tot de onderwereldkrater helpt wetenschappers de klimaatgeschiedenis van de aarde in kaart te brengen
Toegangspoort tot de onderwereldkrater helpt wetenschappers de klimaatgeschiedenis van de aarde in kaart te brengen Australiërs gevangen door bosbranden verteld te laat om te vertrekken
Australiërs gevangen door bosbranden verteld te laat om te vertrekken
Hoofdlijnen
- AI-tool maakt synthetische afbeeldingen van cellen voor verbeterde microscopieanalyse
- Wat is een voorbeeld van een gel?
- Type energie geproduceerd door fotosynthese
- Waar vinden veel van de basislevensfuncties plaats in organismen?
- Wat zijn de 2 aminozuren die elk door één codon worden vertegenwoordigd?
- Bij mensen is het aantal tetrads gevormd tijdens mitose?
- Kraaien en keapapegaaien blijken het nut van objecten te leren, vergelijkbaar met de manier waarop menselijke baby's het doen
- Is Rucula een monocot of dicot?
- Wat zijn 3 onderscheidende kenmerken van Euglenophytes?
- Enzymbiofabrieken om navelstrengbloedtransplantaties te verbeteren

- Met koper gedoteerd zinksulfide verandert omkeerbaar van kleur wanneer het wordt verlicht en kan worden gebruikt in slimme adaptieve vensters
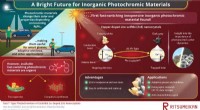
- Een sleutel tot goedkopere hernieuwbare brandstoffen:voorkomen dat ijzer gaat roesten

- Domino-achtige kristallisatie van glas
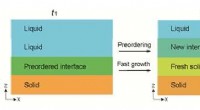
- Van receptorstructuur tot nieuwe osteoporosemedicijnen
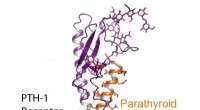
 Welke 5 zuren gebruiken we in ons dagelijks leven?
Welke 5 zuren gebruiken we in ons dagelijks leven?  Is een koninkrijksgroep organismen die in hetzelfde gebied leven?
Is een koninkrijksgroep organismen die in hetzelfde gebied leven?  Zorgt verstedelijking voor de evolutie van planten?
Zorgt verstedelijking voor de evolutie van planten?  Hoe conserveren en herstellen we computergebaseerde kunst in een veranderende technologische omgeving?
Hoe conserveren en herstellen we computergebaseerde kunst in een veranderende technologische omgeving? Welke laag in het binnenste van de aarde is het dunste en welke dichtheid heeft die laag?
Welke laag in het binnenste van de aarde is het dunste en welke dichtheid heeft die laag?  We hebben de taal van Nieuw-Zeelandse Twitter-gebruikers geanalyseerd tijdens de lockdown, met verrassende resultaten
We hebben de taal van Nieuw-Zeelandse Twitter-gebruikers geanalyseerd tijdens de lockdown, met verrassende resultaten Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?
Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?  Wat is Facebook Watch en vind je het leuk?
Wat is Facebook Watch en vind je het leuk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

