
Wetenschap
Welk element zal een edelgasconfiguratie hebben als het een ionische binding vormt door één elektron uit natriumatoom te accepteren?
Het element dat een edelgasconfiguratie heeft als het een ionische binding vormt door één elektron uit een natriumatoom te accepteren, is chloor (CL) .
Dit is waarom:
* natrium (na) Heeft één valentie -elektron. Door dit elektron te verliezen, bereikt het een stabiele edelgasconfiguratie zoals Neon (NE). Dit vormt een positief geladen natriumion (Na+).
* chloor (Cl) heeft zeven valentie -elektronen. Door één elektron te krijgen, bereikt het ook een stabiele edelgasconfiguratie zoals Argon (AR). Dit vormt een negatief geladen chloride-ion (Cl-).
De elektrostatische aantrekkingskracht tussen het positief geladen natriumion en het negatief geladen chloride -ion vormt de ionische binding, wat resulteert in de vorming van natriumchloride (NaCl), ook bekend als tafelzout.
 Suikermoleculen gebruiken om katoenmateriaal te laten gloeien
Suikermoleculen gebruiken om katoenmateriaal te laten gloeien Nieuw scheidingsproces voor belangrijk radiodiagnostisch middel vermindert radioactief afval
Nieuw scheidingsproces voor belangrijk radiodiagnostisch middel vermindert radioactief afval Welk type verandering is nodig om een verbinding af te breken?
Welk type verandering is nodig om een verbinding af te breken?  Wat is de kleur van rood lakmoespapier in zuiveringszout?
Wat is de kleur van rood lakmoespapier in zuiveringszout?  Waarom bevriest zoutwater onder 0 Celsius?
Waarom bevriest zoutwater onder 0 Celsius?
Hoofdlijnen
- Is menselijke ontbinding anaëroob of aëroob?
- Big data helpen bepalen wat het ziekterisico veroorzaakt
- Wat is de studie van hoe genen worden overgedragen van ouders naar hun kinderen en rol bij gezondheidsziekten die bekend staan als?
- Hoe worden eiwitten gevormd door het concept van polymerisatie te gebruiken?
- Mesozoïsche zoogdieren:wat weten we van China?
- Zonder goed beheer raakt de Braziliaanse Cerrado misvormd en minder veerkrachtig tegen de klimaatverandering
- Wat is het dikke buitenmembraan van acoliet?
- Waar komt ons hoofd vandaan?
- Wat is het gebruik van beker?
- Proces verwijdert tegelijkertijd giftige metalen en zout om schoon water te produceren

- Ontwikkeling van elektrodemateriaal dat de efficiëntie van zoutgehaltegradiëntenergie verbetert

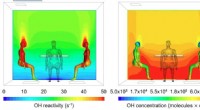
- Een nieuwe kijk op de chemie van de binnenlucht
- Onderzoekers gebruiken schuifkrachten om zelf-geassembleerde supramoleculaire hydrogel te maken

- Besprenkeld met kracht:hoe onzuiverheden een thermo-elektrisch materiaal versterken op atomair niveau

 Wat zijn de vier organische moleculen in levende dingen?
Wat zijn de vier organische moleculen in levende dingen?  Kan iemand elektrisch vanuit uw meter stelen?
Kan iemand elektrisch vanuit uw meter stelen?  Hoe onderzeeërs werken
Hoe onderzeeërs werken  Hoe ziet de aarde eruit vanaf Mars?
Hoe ziet de aarde eruit vanaf Mars?  Op welke temperatuur bevriest het ongelode gas?
Op welke temperatuur bevriest het ongelode gas?  Wat is het oxidatiegetal van calcium?
Wat is het oxidatiegetal van calcium?  Wat maakt Vibgyor -licht om zichtbaar te zijn?
Wat maakt Vibgyor -licht om zichtbaar te zijn?  Wat zijn de verschillen tussen de mineralen Calciet en Quartz?
Wat zijn de verschillen tussen de mineralen Calciet en Quartz?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

