
Wetenschap
Hoe bereken je mol atomen in 9,00 g magnesiumnitraat?
1. Vind de molaire massa magnesiumnitraat:
* Mg:24.31 g/mol
* N:14.01 g/mol (x 2 =28,02 g/mol)
* O:16.00 g/mol (x 6 =96,00 g/mol)
Totale molaire massa van mg (no₃) ₂ =24,31 + 28.02 + 96.00 =148,33 g/mol
2. Bereken de mol magnesiumnitraat:
* mol =massa / molaire massa
* mol =9,00 g / 148,33 g / mol
* mol =0,0607 mol mg (no₃) ₂
3. Bepaal het totale aantal atomen per molecuul:
* Eén molecuul van mg (no₃) ₂ bevat:
* 1 magnesiumatoom (mg)
* 2 stikstofatomen (n)
* 6 zuurstofatomen (O)
* Totaal =9 atomen
4. Bereken de mol atomen:
* mol atomen =mol mg (no₃) ₂ * atomen per molecuul
* mol atomen =0,0607 mol * 9 atomen/molecuul
* mol atomen =0,546 mol
Daarom zijn er ongeveer 0,546 mol atomen in 9,00 g magnesiumnitraat.
 Eetgewoonten van blanke mensen produceren de meeste broeikasgassen
Eetgewoonten van blanke mensen produceren de meeste broeikasgassen Video:Hoe zullen kuststeden zich aanpassen aan de zeespiegelstijging?
Video:Hoe zullen kuststeden zich aanpassen aan de zeespiegelstijging? Zichtbaar vanuit de ruimte, De onofficiële paden van Detroit kunnen een belangrijke rol spelen bij landherontwikkeling
Zichtbaar vanuit de ruimte, De onofficiële paden van Detroit kunnen een belangrijke rol spelen bij landherontwikkeling De VN heeft zojuist een universeel mensenrecht op een gezond, duurzaam milieu uitgeroepen. Waar dit toe kan leiden
De VN heeft zojuist een universeel mensenrecht op een gezond, duurzaam milieu uitgeroepen. Waar dit toe kan leiden De Pacific Garbage Patch uitgelegd -- Nieuwe updates
De Pacific Garbage Patch uitgelegd -- Nieuwe updates
Hoofdlijnen
- Nieuwe hypothese:waarom bacteriën steeds resistenter worden tegen antibiotica
- Hoe dodelijke parasieten ervoor kiezen mannelijk te zijn:Onderzoekers onthullen genexpressie gedurende de levenscyclus van Cryptosporidium
- Wat maken wetenschappers om hen te helpen een hypothese of gegevens te verzamelen tijdens een experiment?
- Wordt Barr Body gevonden in 80 procent polymorfonucleaire leukocyten?
- Als talen botsen, wie overleeft er dan?
- Wat zijn de 4 belangrijkste soorten biologisch macromolecuul?
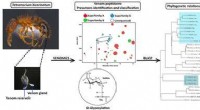
- Hoe binnendringende ziekteverwekkers de afweer van plantencellen uitschakelen
- Het op lange termijn volgen van het voedselgedrag van walvissen via satelliet is nu mogelijk met nieuwe tag
- Wat is een organisme dat de hele of een andere roept doodt en eet?
- Mieren geven hun giftige geheimen prijs
- Geowetenschappers onthullen ijzige kristalstructuren van hagelstenen

- Forensische wetenschappers herstellen menselijk DNA van muggen

- Henneptestlab gelanceerd als antwoord op de behoefte van de industrie

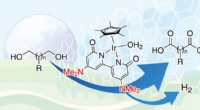
- Team synthetiseert gelijktijdig dicarbonzuren en waterstof uit diolen
 Groeiende metalen kristallen in vloeibaar metaal
Groeiende metalen kristallen in vloeibaar metaal Uit welke 2 stoffen bestaat zout?
Uit welke 2 stoffen bestaat zout?  Wat is natte lucht?
Wat is natte lucht?  Zwavel in elke porie:verbeterde batterijen met koolstofnanodeeltjes
Zwavel in elke porie:verbeterde batterijen met koolstofnanodeeltjes Britse bedrijfsreuzen ondertekenen pact om plastic afval te verminderen
Britse bedrijfsreuzen ondertekenen pact om plastic afval te verminderen Hoe groot is een stellaire nevel?
Hoe groot is een stellaire nevel?  Origami inspireert onderzoek naar materialen die zichzelf assembleren bij blootstelling aan licht (met video)
Origami inspireert onderzoek naar materialen die zichzelf assembleren bij blootstelling aan licht (met video) Nieuw boek ontkracht mythen over wie misdaad veroorzaakt en waarom
Nieuw boek ontkracht mythen over wie misdaad veroorzaakt en waarom
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

