
Wetenschap
Hoeveel valentie -elektronen verliezen alkali -metalen om een octet te verkrijgen?
Dit is waarom:
* valentie -elektronen: Alkali -metalen bevinden zich in groep 1 van de periodiek systeem. Dit betekent dat ze één hebben valentie -elektron in hun buitenste schaal.
* octetregel: De octetregel stelt dat atomen de neiging hebben om elektronen te winnen, verliezen of delen om een stabiele configuratie van acht elektronen in hun buitenste schaal te bereiken.
* Een elektron verliezen: Door hun enkele valentie -elektron te verliezen, bereiken alkali -metalen de elektronenconfiguratie van het edelgas in de vorige periode. Deze configuratie heeft een volledig octet in de buitenste schaal, waardoor het atoom stabiel is.
Voorbeeld: Natrium (NA) heeft één valentie -elektron. Wanneer het dit elektron verliest, wordt het een positief geladen ion (Na+) met dezelfde elektronenconfiguratie als de Noble Gas Neon (NE), die een volledig octet heeft.
 Wegenkaart schetst hindernissen bij de ontwikkeling van kathodes van de volgende generatie voor het aandrijven van elektrische voertuigen
Wegenkaart schetst hindernissen bij de ontwikkeling van kathodes van de volgende generatie voor het aandrijven van elektrische voertuigen Hoe crack-cocaïne werkt
Hoe crack-cocaïne werkt  Hoe een coördinatienummer te berekenen
Hoe een coördinatienummer te berekenen  Wat wordt gebruikt om de cilinder in het laboratorium te meten?
Wat wordt gebruikt om de cilinder in het laboratorium te meten?  Smelt een ijsblokje sneller in olie of water?
Smelt een ijsblokje sneller in olie of water?
Hoofdlijnen
- Welke kenmerken worden gebruikt om organismen te classificeren in domeinen en koninkrijken?
- Het verlenen van rechtspersoonlijkheid aan de natuur is een groeiende beweging:kan dit het verlies aan biodiversiteit tegengaan?
- Waarom ademen mensen op de planeet Aarde?
- Welke drie letters eindigen op een woord geven aan dat het molecuul suiker is?
- Wat betekent dierenactie in de wetenschap?
- Wat welke koninkrijk prokaryoten?
- In planten hebben gymnospermen kegels en angiospermen bloemen. Beide plantenstructuren zijn waarvoor gespecialiseerd?
- Microben reizen door de lucht; Het zou goed zijn om te weten hoe en waar
- Hoe wordt het ene geslacht groter dan het andere?
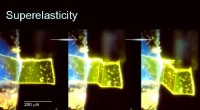
- Toekomstige auto's kunnen gemaakt worden van revolutionair nieuw materiaal

- Binnenkort:een bloedtest voor de ziekte van Alzheimer?

- Kan een stromend vloeistofachtig materiaal zijn structurele orde handhaven zoals kristallen?

- Plastic transparanter maken en tegelijkertijd elektrische geleidbaarheid toevoegen

- Rood licht voor stress:een van kleur veranderend organisch kristal
 Mariene organismen kunnen een plastic zak in 1,75 miljoen stukjes versnipperen, studie toont
Mariene organismen kunnen een plastic zak in 1,75 miljoen stukjes versnipperen, studie toont Hoe beïnvloedt een temperatuurstijging het vermogen van een gas om in oplossing te gaan?
Hoe beïnvloedt een temperatuurstijging het vermogen van een gas om in oplossing te gaan?  Gestrande Noord-Caroliniërs maken de balans op van de schade van de Doriërs
Gestrande Noord-Caroliniërs maken de balans op van de schade van de Doriërs Het Mars-monsterproject speelt een grote rol in de laatste besprekingen over de uitgaven
Het Mars-monsterproject speelt een grote rol in de laatste besprekingen over de uitgaven  Wat is het verschil tussen een proton en een waterstofion?
Wat is het verschil tussen een proton en een waterstofion?  Wat houdt DNA in de kern die wordt omsloten door zijn eigen membraan?
Wat houdt DNA in de kern die wordt omsloten door zijn eigen membraan?  T-Mobile belooft consumentenvoordelen als Sprint-deal OKd
T-Mobile belooft consumentenvoordelen als Sprint-deal OKd Rekbare supercondensatoren om de draagbare apparaten van morgen van stroom te voorzien
Rekbare supercondensatoren om de draagbare apparaten van morgen van stroom te voorzien
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

