
Wetenschap
Elementen en verbindingen verlaten de oplossingen tijdens het koelen Wat als mineralen?
Hier is een uitsplitsing:
* Oplossing: Een homogene mengsel van een opgeloste stof (de stof die wordt opgelost) en een oplosmiddel (de stof die het oplossen doet).
* Koeling: Naarmate een oplossing afkoelt, neemt de oplosbaarheid van de opgeloste stoffen af. Dit betekent dat minder van de opgeloste stof in het oplosmiddel kan blijven opgelost.
* neerslag: De overtollige opgeloste stof, die niet opgelost kan blijven, komt uit de oplossing en vormt een vaste stof. Deze vaste stof kan de vorm aannemen van kristallen, die regelmatig zijn, herhalende regelingen van atomen of moleculen.
* Mineraal: Een natuurlijk voorkomende vaste stof met een gedefinieerde chemische samenstelling en een karakteristieke kristalstructuur.
Voorbeeld:
* zout water: Zout (NaCl) opgelost in water.
* Koeling: Terwijl het zoutwater afkoelt, neemt de oplosbaarheid van zout af.
* neerslag: Een deel van het zout gaat uit de oplossing als kristallen.
* Mineraal: De neergeslagen zoutkristallen zijn het minerale haliet (NaCl).
Andere factoren die neerslag beïnvloeden:
* concentratie: Hogere concentraties van opgeloste stoffen leiden tot meer neerslag.
* Verdamping: Verdamping van het oplosmiddel kan ook neerslag veroorzaken.
* nucleatie -sites: De aanwezigheid van oppervlakken of onzuiverheden kan fungeren als nucleatieplaatsen, waardoor kristalgroei wordt aangemoedigd.
Belangrijke opmerking: Niet alle neerslag leidt tot minerale vorming. Sommige stoffen kunnen uit oplossing neerslaan als amorfe vaste stoffen (zonder een gewone kristalstructuur) of als niet-minerale materialen.
 Onderzoekers beoordelen gebruik, fytochemie en farmacologische eigenschappen van het geslacht Blechnum
Onderzoekers beoordelen gebruik, fytochemie en farmacologische eigenschappen van het geslacht Blechnum Welke pH -klep meet de zuurgraad?
Welke pH -klep meet de zuurgraad?  Niet-invasieve magnetische resonantiebeeldvorming van longfibrogenese met een op aminozuren gerichte sonde
Niet-invasieve magnetische resonantiebeeldvorming van longfibrogenese met een op aminozuren gerichte sonde Hoe teken je een ionische binding van lithium en aluminium?
Hoe teken je een ionische binding van lithium en aluminium?  Zit butaan in groep 2 van het periodiek systeem?
Zit butaan in groep 2 van het periodiek systeem?
Hoofdlijnen
- Wat wordt er gevonden in de kieuwen van champignons?
- Hoe wordt de kloof tussen tanden van een herbivoor genoemd?
- Welke 3 elementen worden gevonden in alle biologische macromoleculen?
- Waarom eten honden kak en hoe u uw huisdier kunt laten stoppen
- Waarom gebaren we?
- Hoe vermeld je twee soorten levende wezens beschrijven kort hoe ze anders en vergelijkbaar zijn?
- Wat is het verschil tussen dieren- en bacteriecellen?
- Woordproblemen schrijven voor Math
- Orka's leren elkaar hoe ze vis kunnen stelen uit de menselijke visserij
- Kun je een malt whisky van 10 jaar maken in weken? De chemie zegt ja

- Wetenschappers bij ESS, Zweeds wateronderzoek, ORNL gebruikt VISION om te kijken naar veelvoorkomende verontreinigingen voor toepassingen in schoner water

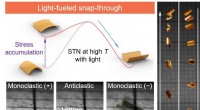
- Moleculaire schakelaar maakt fotomechanisch springen van polymeren mogelijk
- Metalen organische raamwerken gemaakt om als vloeistof te fungeren

- Nieuw inzicht in het trainen van zeer reactieve chemische verbindingen

 Onderzoekers ontwikkelen CRISPR om enkele RNA-letters in menselijke cellen te bewerken
Onderzoekers ontwikkelen CRISPR om enkele RNA-letters in menselijke cellen te bewerken 2040:Hoop en actie in de klimaatcrisis
2040:Hoop en actie in de klimaatcrisis Twee- tot drievoudige toename van het optreden en de ernst van hittegolven, direct te zien in temperatuurrecords in het VK
Twee- tot drievoudige toename van het optreden en de ernst van hittegolven, direct te zien in temperatuurrecords in het VK Wetenschappers geven nieuwe verklaring voor de vreemde asymmetrie van de maan
Wetenschappers geven nieuwe verklaring voor de vreemde asymmetrie van de maan NASA-NOAA satellietanimatie toont het einde van tropische cycloon Boris
NASA-NOAA satellietanimatie toont het einde van tropische cycloon Boris De menselijke factor beperkt de hoop op klimaatoplossingen
De menselijke factor beperkt de hoop op klimaatoplossingen Nieuw lenssysteem voor helderder, scherpere diffractiebeelden
Nieuw lenssysteem voor helderder, scherpere diffractiebeelden Circulair gepolariseerde luminescentie van organische micro-/nanostructuren
Circulair gepolariseerde luminescentie van organische micro-/nanostructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

