Wetenschap
Wat is de som van pH en POH in een oplossing?
De som van pH en POH in elke oplossing is altijd 14 .
Dit is gebaseerd op de volgende relatie:
* KW =[H+] [OH-] =1,0 x 10^-14
Waar:
* KW is de ionenproductconstante van water.
* [H+] is de concentratie waterstofionen.
* [OH-] is de hydroxide-ionenconcentratie.
Het nemen van de negatieve logaritme van beide zijden van de vergelijking:
* -log (KW) =-log ([H+] [OH-])
* PKW =Ph + POH
Omdat PKW gelijk is aan 14, zal de som van de pH en POH altijd 14 zijn.
 Onthulling van het effect van Ti-substituties op het statische oxidatiegedrag van (Hf,Ti)C bij 2500°C
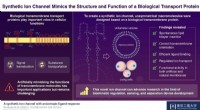
Onthulling van het effect van Ti-substituties op het statische oxidatiegedrag van (Hf,Ti)C bij 2500°C  Onderzoekers printen kanaalstructuren in kwartsglas
Onderzoekers printen kanaalstructuren in kwartsglas Welk element wordt gevonden in alle organische verbindingen en levende orginismen?
Welk element wordt gevonden in alle organische verbindingen en levende orginismen?  Wat is het resultaat van het toevoegen van loodnitraat aan kaliumjodide?
Wat is het resultaat van het toevoegen van loodnitraat aan kaliumjodide?  Een oplossing met een hoge concentratie van niet-afnemende opgeloste stoffen wordt genoemd?
Een oplossing met een hoge concentratie van niet-afnemende opgeloste stoffen wordt genoemd?
Hoofdlijnen
- Make-up wetenschapsprojecten
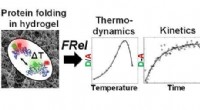
- Wat is het belang van enzymen in een biologisch proces?
- Onderzoeker stelt antwoord voor waarom grotdieren blind worden
- Wat is de rol van diffusie in een cel?
- Welk onderdeel van de biosfeer is een voorbeeld anorganische materie A. Suikers en NBSP B. Eiwitten C. Koolhydraten D. Mineralen?
- Europa's oudste boom groeit nog steeds
- Wat doet acetonalcohol met een gramkleuring?
- Hoe functioneert structuur -affactfunctie in de biologie?
- Een bouwsteen voor leverfitness op oudere leeftijd
 Wat is harder granieten kalksteenmarmeren of diamant?
Wat is harder granieten kalksteenmarmeren of diamant?  Wat is de druk in atmosferen van een 0,108 molmonster heliumgas bij temperatuur 20 Celsius als het volume 0,505L is?
Wat is de druk in atmosferen van een 0,108 molmonster heliumgas bij temperatuur 20 Celsius als het volume 0,505L is?  Hoe een zuurstofatoom maken Replica
Hoe een zuurstofatoom maken Replica Wie heeft oorspronkelijk het concept voorgesteld dat materie bestaat uit kleine ondeelbare deeltjes?
Wie heeft oorspronkelijk het concept voorgesteld dat materie bestaat uit kleine ondeelbare deeltjes?  Wat zijn de belangrijke voordelen van wetenschap en technologie?
Wat zijn de belangrijke voordelen van wetenschap en technologie?  Ondergrondse anomalie gevonden nabij iconisch piramidecomplex van Gizeh
Ondergrondse anomalie gevonden nabij iconisch piramidecomplex van Gizeh  Vormen chloor en natrium een verbinding?
Vormen chloor en natrium een verbinding?  Een voet converteren naar vierkanten voet
Een voet converteren naar vierkanten voet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com