
Wetenschap
Hoeveel mol CO2 vormen zich wanneer 58 gram butaan C4H10 in zuurstof verbrandt?
1. Schrijf de gebalanceerde chemische vergelijking:
2 c₄h₁₀ + 13 o₂ → 8 co₂ + 10 h₂o
2. Bereken de molaire massa van butaan (c₄h₁₀):
Molaire massa van C =12,01 g/mol
Molaire massa van h =1,01 g/mol
Molaire massa van C₄h₁₀ =(4 * 12.01) + (10 * 1.01) =58.12 g/mol
3. Converteer gram van butaan in mollen:
Mol c₄h₁₀ =(58 g) / (58,12 g / mol) =1 mol
4. Gebruik de molverhouding van de gebalanceerde vergelijking:
De gebalanceerde vergelijking toont aan dat 2 mol C₄h₁₀ 8 mol co₂ produceert. Daarom is de molverhouding 2:8 of 1:4.
5. Bereken mol van co₂ geproduceerd:
Mol co₂ =(1 mol c₄h₁₀) * (4 mol co₂ / 1 mol c₄h₁₀) =4 mol co₂
Antwoord: 4 mol co₂ vormt wanneer 58 gram butaan in zuurstof verbrandt.
Hoofdlijnen
- Een organisme dat eigen voedsel maakt?
- Hoe de schedel van de oudst bekende voorouder van de mensheid ons begrip van de evolutie verandert
- Hoe natuurkunde en biologie samenwerken om de mechanismen van het leven te verkennen
- Genoomsequencing onthult uitgebreide inteelt bij Scandinavische wolven
- Welke soorten moleculen kunnen door het plasmamembraan worden gevoerd door eenvoudige diffusie?
- Wat zijn genetische vergelijkingen?
- Wetenschappers vinden ontbrekende schakel om te begrijpen hoe planten vitamine C aanmaken
- Genetisch gemodificeerde paarse tomaten komen mogelijk naar een Amerikaanse supermarkt bij jou in de buurt
- Kan de wetenschap bendemoorden voorspellen?
- Iridium-gekatalyseerde Z-retentieve asymmetrische allylische substitutiereacties
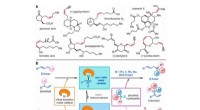
- Het toevoegen van een polymeer stabiliseert instortende metaal-organische raamwerken

- De geur van pure chocolade, gedemystificeerd
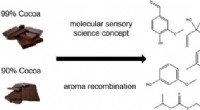
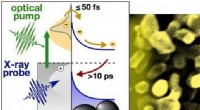
- Wetenschappers maken spontane snapshots van elektronen die licht oogsten op atomaire schaal
- Machine learning gebruiken om peptiden te ontwerpen
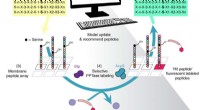
 Nieuwe exploitatietechnieken en verdedigingen voor DOP-aanvallen
Nieuwe exploitatietechnieken en verdedigingen voor DOP-aanvallen Nieuw onderzoek geeft aanwijzingen over hoe continenten vroeg in de geschiedenis van de aarde ontstonden (met video)
Nieuw onderzoek geeft aanwijzingen over hoe continenten vroeg in de geschiedenis van de aarde ontstonden (met video)  Wie heeft de mogelijkheid om lichte energie om te zetten in chemische energie?
Wie heeft de mogelijkheid om lichte energie om te zetten in chemische energie?  Economische impact van kusterosie
Economische impact van kusterosie Hoe ongelijkheden op te lossen
Hoe ongelijkheden op te lossen Wat maakt moeraslichamen anders dan woestijnmummies?
Wat maakt moeraslichamen anders dan woestijnmummies?  Heeft een surfer de theorie van alles ontdekt?
Heeft een surfer de theorie van alles ontdekt?  Welke verandering zou optreden als de rotatiesnelheid aanzienlijk afnam?
Welke verandering zou optreden als de rotatiesnelheid aanzienlijk afnam?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


