
Wetenschap
Waarom is aspirine reactiever dan benzeen?
* Benzeen's aromatische stabiliteit: Benzeen heeft een zeer stabiele structuur vanwege zijn gedelokaliseerde PI -elektronen, waardoor een resonantie hybride ontstaat. Deze delocalisatie maakt het minder vatbaar voor elektrofiele aanval, wat de typische manier is waarop aromatische verbindingen reageren.
* Aspirin's functionele groepen: Aspirine heeft verschillende functionele groepen die het reactiever maken dan benzeen. Deze omvatten:
* carbonzuurgroep: De carbonzuurgroep (-COOH) is zuur en vatbaar voor reacties zoals verestering, amidatie en zoutvorming.
* Estergroep: De estergroep (-coo-) kan hydrolyse en andere reacties ondergaan.
* Elektrofiele aanval: Hoewel benzeen elektrofiele aromatische substitutie kan ondergaan, vereist het zware omstandigheden en sterke elektrofielen. Aspirine is met zijn functionele groepen gevoeliger voor elektrofiele aanval onder mildere omstandigheden.
Samenvattend: De aromatische stabiliteit van Benzeen maakt het minder reactief, terwijl de functionele groepen van aspirine zijn reactiviteit verhogen. Daarom is aspirine reactiever dan benzeen.
 Een test van 25 minuten kan de eerste diagnose van urineweginfecties vereenvoudigen, strijd tegen antibioticaresistentie
Een test van 25 minuten kan de eerste diagnose van urineweginfecties vereenvoudigen, strijd tegen antibioticaresistentie Chemici leren hoe ze fenolen in gerookte voedselmonsters kunnen detecteren met behulp van vitamine B4
Chemici leren hoe ze fenolen in gerookte voedselmonsters kunnen detecteren met behulp van vitamine B4  Onderzoekers stroomlijnen moleculaire assemblagelijn om te ontwerpen, test medicijnverbindingen
Onderzoekers stroomlijnen moleculaire assemblagelijn om te ontwerpen, test medicijnverbindingen Welke van de volgende formules stelt een aldehyde a c6h10o5 b c2h4o c c2h5oh d ch3cooh voor?
Welke van de volgende formules stelt een aldehyde a c6h10o5 b c2h4o c c2h5oh d ch3cooh voor?  Het AI-model vergelijkt rechtstreeks de eigenschappen van potentiële nieuwe medicijnen
Het AI-model vergelijkt rechtstreeks de eigenschappen van potentiële nieuwe medicijnen
Hoofdlijnen
- Uit onderzoek blijkt hoe cellen schadelijke extra kopieën van DNA voorkomen
- Wat zijn de juiste reeksen gebeurtenissen in productie -recombinant DNA?
- Cultuur kan verklaren waarom hersenen groter zijn geworden
- Wat versta je onder osmose?
- Seizoensregulatie in de biologische klok van de bonenbughersenen
- Wat zijn medorieten?
- Studie onthult hoe DNA zich ontvouwt voor transcriptie
- Uitleggen hoe de hersenen gezichten herkennen
- Pas op voor de huisdieren bij het hanteren van de Halloween-snoepvangst
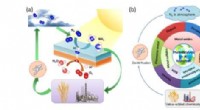
- Fotochemische stikstoffixatie - nieuwe perspectieven openen voor een toekomst met duurzame energie
- Malaria kan worden geveld door een Antarctische zeespons

- Kristallen die aardgas zuiveren

- Sporen van opiaten gevonden in oud Cypriotisch schip

- Productie van drop-in brandstof uit biomassa door microbiële en elektrochemische conversie

 Wat zou er gebeuren met de frequentie van eclipsen als een baan niet werd gekanteld?
Wat zou er gebeuren met de frequentie van eclipsen als een baan niet werd gekanteld?  Gedeeld overlevingsmechanisme verklaart waarom 'goede' zenuwcellen blijven bestaan en 'slechte' kanker floreert
Gedeeld overlevingsmechanisme verklaart waarom 'goede' zenuwcellen blijven bestaan en 'slechte' kanker floreert  Hoe zwaar is donkere materie? Wetenschappers verkleinen voor het eerst het potentiële massabereik radicaal
Hoe zwaar is donkere materie? Wetenschappers verkleinen voor het eerst het potentiële massabereik radicaal Wetenschappers vinden een vroeg moment dat wijst op een komende megabeving
Wetenschappers vinden een vroeg moment dat wijst op een komende megabeving Verbetering van de waterkwaliteit van Lake Eries
Verbetering van de waterkwaliteit van Lake Eries Vijf kenmerken van de wetenschappelijke methode
Vijf kenmerken van de wetenschappelijke methode  Hoe lees je theorie -antwoorden?
Hoe lees je theorie -antwoorden?  Om online debatten te winnen, sociale netwerken die duizend woorden waard zijn
Om online debatten te winnen, sociale netwerken die duizend woorden waard zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

