
Wetenschap
Hoe wordt een atoomspectra geproduceerd?
1. De atomen opwindend
* Energieabsorptie: Atomen in hun grondtoestand (laagste energieniveau) absorberen energie. Dit kan door verschillende methoden gebeuren:
* Verwarming: Een elektrische stroom door een gas doorgeven, een vlam met behulp van een vlam of het monster blootstellen aan hoge temperaturen.
* Elektrische ontlading: Een hoge spanning op een gas toepassen.
* bombardement: Een straal elektronen of fotonen gebruiken om de atomen te slaan.
* energieniveaus: De geabsorbeerde energie bevordert elektronen van hun grondtoestand naar hogere energieniveaus (geëxciteerde toestanden). Deze geëxciteerde staten zijn onstabiel.
2. Emissie van licht
* ontspanning: De opgewonden elektronen gaan snel terug naar lagere energieniveaus.
* fotonemissie: Terwijl een elektron van een hoger energieniveau naar een lager daalt, brengt het de overtollige energie af als een foton van licht. De energie van het foton komt precies overeen met het energieverschil tussen de twee niveaus.
* specifieke golflengten: Elk element heeft een unieke set energieniveaus, wat resulteert in de emissie van licht bij specifieke golflengten. Dit is de basis voor atomaire spectroscopie, die elementen in een monster kunnen identificeren.
3. Het spectrum observeren
* spectroscoop: Een apparaat dat een spectroscoop wordt genoemd, scheidt het uitgezonden licht in de golflengten van de component.
* Spectrale lijnen: Het uitgezonden licht verschijnt als heldere lijnen (emissiespectrum) bij specifieke golflengten, die de energieverboorzers binnen het atoom vertegenwoordigen.
* absorptiespectrum: Als het licht door een monster van atomen gaat, absorberen de atomen licht bij specifieke golflengten die overeenkomen met hun energieverzochten. Dit resulteert in donkere lijnen (absorptiespectrum) tegen een continue achtergrond.
Key Concepts
* kwantisatie: Atomen kunnen alleen bestaan in specifieke energieniveaus. Energieovergangen tussen deze niveaus zijn discreet, wat resulteert in specifieke golflengten van licht.
* Quantummodel: Het concept van gekwantiseerde energieniveaus verklaart waarom elk element een uniek atoomspectrum heeft.
Toepassingen
* Identificerende elementen: Atomische spectra zijn als vingerafdrukken voor elementen, waardoor wetenschappers hun aanwezigheid en samenstelling in verschillende monsters kunnen identificeren.
* Astrophysics: Spectra van sterren en andere hemelse objecten onthullen hun chemische samenstelling, temperatuur en beweging.
* Analytische chemie: Atomische spectroscopie wordt gebruikt voor kwantitatieve analyse op verschillende gebieden, zoals milieumonitoring, voedselwetenschap en klinische chemie.
 Tyrosinechassis voor duurzame productie met hoog rendement van nuttige verbindingen in slimme gistcellen
Tyrosinechassis voor duurzame productie met hoog rendement van nuttige verbindingen in slimme gistcellen Zacht maar sterk:biohybride materiaal presteert als kraakbeen
Zacht maar sterk:biohybride materiaal presteert als kraakbeen Oude eiwitten in detail bestudeerd
Oude eiwitten in detail bestudeerd In welke mate bevriest zoutwater in ijs?
In welke mate bevriest zoutwater in ijs?  Groene waterstof produceren door blootstelling van nanomaterialen aan zonlicht
Groene waterstof produceren door blootstelling van nanomaterialen aan zonlicht
 Gemeenschappelijke Mississippi Spiders
Gemeenschappelijke Mississippi Spiders  Sommige zoetwatermosselen blijven in gevaar. Hoe?
Sommige zoetwatermosselen blijven in gevaar. Hoe?  China haast zich om overstromingen in te dammen na recordregen
China haast zich om overstromingen in te dammen na recordregen Koolstofbelasting krijgt hernieuwde aandacht, maar stuit nog steeds op weerstand
Koolstofbelasting krijgt hernieuwde aandacht, maar stuit nog steeds op weerstand Hoe onderzoekers, boeren en brouwers bier willen beschermen tegen klimaatverandering
Hoe onderzoekers, boeren en brouwers bier willen beschermen tegen klimaatverandering
Hoofdlijnen
- Pogingen om te vangen, red het bedreigde einde van de bruinvis in Mexico
- Bij voetbalsucces draait alles om vaardigheid:studeren
- Wat betekent de deelresultaten in de wetenschappelijke methode?
- Wat zijn vier hoofdtypen macromoles die in levende wezens worden gevonden?
- Uitgestorven houtetende kakkerlak na 80 jaar herontdekt
- Mysterie CRISPR ontgrendeld:een nieuwe bondgenoot tegen antibioticaresistentie?
- Wat is zymotechnologie?
- Beschrijving van de basisfuncties van enzymen in cellen
- Ideeën voor wetenschapsbeurzen Projecten met honden
- Ontwerpen van biologische beweging op nanometerschaal

- Kunstmatige en biologische cellen werken samen als mini-chemische fabrieken

- Lab onthult nieuw werkingsmechanisme tegen SARS-CoV-2 door antiviraal medicijn remdesivir

- Nieuw materiaal breekt wereldrecord voor het omzetten van warmte in elektriciteit

- Productie recyclebaar plastic stap dichterbij
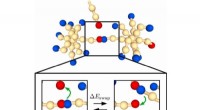
 Hoe denk je dat kristallen met meer onzuiverheden eruit zullen zien in vergelijking met een minder onzuiverheden?
Hoe denk je dat kristallen met meer onzuiverheden eruit zullen zien in vergelijking met een minder onzuiverheden?  Seizoensvariabiliteit in milieuprocessen van meren onthullen gevoeligheid voor klimaatverandering
Seizoensvariabiliteit in milieuprocessen van meren onthullen gevoeligheid voor klimaatverandering Wat zijn voorbeelden van mechanische verwering?
Wat zijn voorbeelden van mechanische verwering?  Nieuwe nanostructuren voor efficiënt energietransport over lange afstand
Nieuwe nanostructuren voor efficiënt energietransport over lange afstand Geschiedenis van het dumpen van DDT-oceaan voor de kust van LA nog erger dan verwacht, vindt EPA
Geschiedenis van het dumpen van DDT-oceaan voor de kust van LA nog erger dan verwacht, vindt EPA Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten
Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten Magelhaense wolken bewijzen dat het nooit te laat is om actief te worden
Magelhaense wolken bewijzen dat het nooit te laat is om actief te worden Een ultrasnelle microscoop voor de kwantumwereld
Een ultrasnelle microscoop voor de kwantumwereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

