
Wetenschap
Waarom beryllium vormt amfoterisch oxide?
* klein formaat en hoge ladingsdichtheid van be²⁺ ion: Beryllium heeft een kleine ionische straal en een hoge ladingsdichtheid. Dit leidt tot een sterke polarisatie van het be²⁺ ion, waardoor het zeer elektronegatief is. Met deze hoge elektronegativiteit kan BEO fungeren als een zuur door elektronenparen te accepteren.
* Hoge ionisatie -energie: Beryllium heeft een zeer hoge ionisatie -energie, waardoor het moeilijk is om elektronen te verliezen en kationen te vormen. Dit draagt bij aan zijn vermogen om covalente bindingen met zuurstof te vormen, wat resulteert in een gedeeltelijk covalent karakter in BEO.
* Polaire covalente aard van Beo: De be-o-binding in Beo is zeer polair vanwege het elektronegativiteitsverschil tussen beryllium en zuurstof. Met deze polariteit kan Beo als basis fungeren door elektronenparen te doneren.
Amfoterische aard in actie:
* als basis: Beo reageert met zuren om zouten en water te vormen:
Beo + 2hcl → Becl₂ + h₂o
* als zuur: Beo reageert met sterke bases om beryles te vormen:
Beo + 2naoh → na₂beo₂ + h₂o
Samenvatting:
De amfoterische aard van berylliumoxide komt voort uit de unieke combinatie van zijn kleine omvang, hoge ladingsdichtheid, hoge ionisatie-energie en het polaire covalente karakter van de BE-O-binding. Hierdoor kan Beo reageren met zowel zuren als basen, wat het dubbele gedrag aantoont.
Hoofdlijnen
- Wie zijn de verschillende biologen en hun bijdragen aan de ontwikkeling van de biologische biotechnologie?
- Hoe zijn cellen, weefsels en organen aan elkaar gerelateerd?
- Waarin verschilt DNA van RNA?
- Intracellulaire expressie - waarom transporteiwitmoleculen remmen hebben
- Oudste chimpansee van bekende Guinese groep sterft
- Verschuivende aanwezigheid van Noord-Atlantische walvissen gevolgd met passieve akoestiek
- Hoe polyfasische slaap werkt
- Noem de Tubluar -klieren die worden gevonden tussen bases van darmvilli?
- Pakken of niet aaien? Hoe de interactie tussen kinderen en honden veilig te houden
- Nieuw ontwikkelde COVID-19-test detecteert en identificeert specifieke varianten met 100% nauwkeurigheid
- Tellurium maakt het verschil

- Onderzoekers ontwikkelen nieuwe elektrodestructuur voor secundaire batterij in vaste toestand

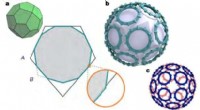
- Onderzoekers creëren onmogelijke eiwitkooien van nanoformaat met behulp van goud
- Onderzoekers creëren een nieuwe klasse van snelheidsgevoelige mechanische metamaterialen

 Vertraging van de Noord-Atlantische circulatie schudde het klimaat van het oude Noord-Europa op
Vertraging van de Noord-Atlantische circulatie schudde het klimaat van het oude Noord-Europa op Is base endotherm of exotherm?
Is base endotherm of exotherm?  Een wet alleen voor het presidentschap van Trump? Californische maatregel heeft tot doel het milieu van staten te beschermen
Een wet alleen voor het presidentschap van Trump? Californische maatregel heeft tot doel het milieu van staten te beschermen Welk type sporen produceert Selanginella?
Welk type sporen produceert Selanginella?  Vechten of vluchten? Waarom individuen reageren zoals ze doen?
Vechten of vluchten? Waarom individuen reageren zoals ze doen? Wat zou de elektronenconfiguratie zijn voor element 118?
Wat zou de elektronenconfiguratie zijn voor element 118?  Wat ontbindt gemiddeld in Math?
Wat ontbindt gemiddeld in Math?  Door aardbevingen geteisterd deel van Kroatië ziet gapende zinkgaten ontstaan
Door aardbevingen geteisterd deel van Kroatië ziet gapende zinkgaten ontstaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


