
Wetenschap
Cellulaire recycling op heterdaad betrapt
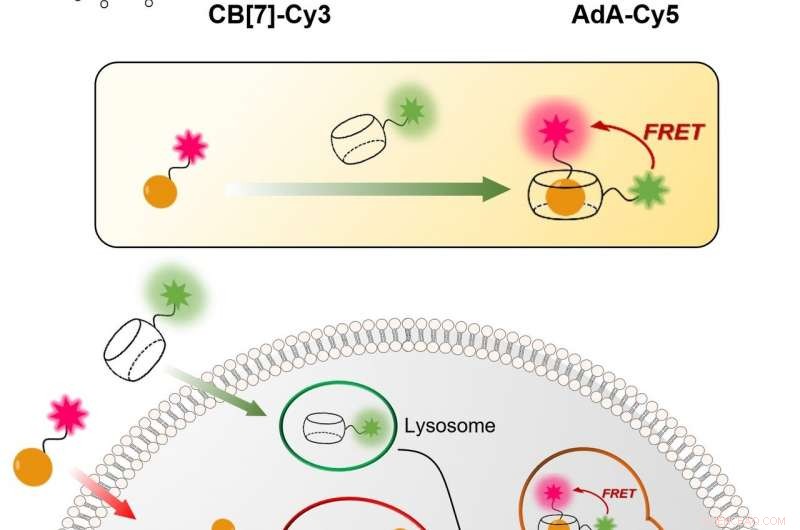
Figuur 1:relatief eenvoudige en goedkope techniek om het cellulaire recyclingmechanisme (autofagie) in realtime te visualiseren. Het proces is gebaseerd op de binding tussen CB[7] en AdA. CB[7] is gebonden aan de fluorescerende kleurstof Cy3 (groen gekleurd) en komt de lysosomen binnen, terwijl AdA is gebonden aan de fluorescerende Cy5 (rood gekleurd) die zich ophoopt in mitochondriën. In het autofagieproces de twee celorganellen smelten samen, wat leidde tot de ontmoeting van CB[7] en AdA. De wetenschappers kunnen de fusie detecteren, want als de twee fluorescerende kleurstoffen dichterbij komen, ze interageren met elkaar via het mechanisme van fluorescentieresonantie-energieoverdracht (FRET). Op deze manier, het onderzoeksteam kan het autofagieproces stap voor stap analyseren. Krediet:Instituut voor Basiswetenschappen
Een team van onderzoekers van het Center for Self-assembly and Complexity, binnen het Instituut voor Basiswetenschappen (IBS) een normaal fysiologisch proces hebben waargenomen, "zelfetend" genoemd, die cellen gebruiken om hun componenten te recyclen. Ze ontwikkelden een nauwkeurige techniek die visualiseert hoe mitochondriën, energiefabrieken van cellen, zijn gefuseerd met lysosomen, de recyclingmachines van cellen, om materiaal vernietigd en gerecycled te krijgen. Aangezien onregelmatigheden in dit mechanisme kunnen leiden tot de ziekte van Alzheimer, Parkinson, en andere complicaties, dit onderzoek zou toekomstige vorderingen in de diagnose van degeneratieve hersenziekten en de ontwikkeling van geneesmiddelen kunnen helpen. De studie is gepubliceerd in Internationale editie van Angewandte Chemie .
De naam "autofagie" komt uit de Griekse taal en betekent "zelfetend". Hoe raar het ook klinkt, het is een onmisbaar proces dat wordt gebruikt om cellen te reinigen van beschadigde organellen en eiwitten. Binnen lysosomen, oude celdelen worden afgebroken tot hun bouwstenen, die worden gebruikt om nieuwe te bouwen. Onlangs, autofagie werd een zeer actief vakgebied en stond in 2016 centraal bij Yoshinori Ohsumi's Nobelprijs voor Fysiologie of Geneeskunde.
Een voorbeeld van een cellulair organel dat periodiek moet worden gerecycled, is het mitochondrion. De zorgvuldige regulering van dit proces is essentieel, en cellen die zich niet regelmatig delen, zoals zenuwcellen, zijn bijzonder kwetsbaar. Als cellen defecte mitochondriën accumuleren, ze kunnen zichzelf beschadigen. Dit komt voor, bijvoorbeeld, bij de ziekte van Alzheimer en Parkinson, waar de opbouw van beschadigde mitochondriën en geaggregeerde eiwitten leidt tot neuronale dood.
Het is bekend dat autofagie (of mitofagie, in het specifieke geval van mitochondriën) gebeurt door fusie van twee verschillende organellen, in dit geval:mitochondriën en lysosomen. Echter, het observeren van het gedrag en de fusie van mitochondriën en lysosomen in de cellen was een uitdaging. Daten, de meeste van deze onderzoeken zijn gebaseerd op fluorescerende eiwitten die aan één organel zijn bevestigd, waardoor de wetenschappers slechts één organel tegelijk kunnen observeren. Bovendien, fluorescerende eiwitten zelf worden afgebroken tijdens autofagie, waardoor het moeilijk is om het mechanisme nauwkeurig te bestuderen.
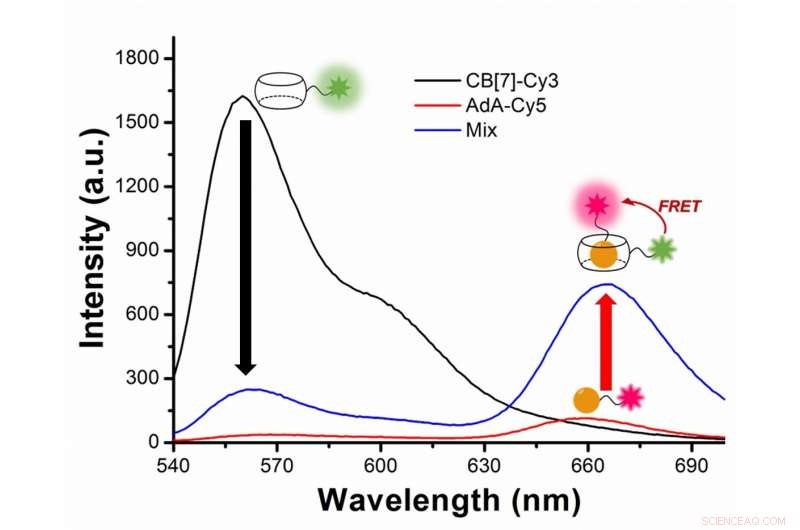
Figuur 2:autofagie bestuderen met fluorescentieresonantie-energieoverdracht (FRET) tussen de groenachtige fluorescerende kleurstof Cy3 en de rode fluorescerende kleurstof Cy5. Cy3 zendt fluorescentie uit met een piekgolflengte bij 563 nanometer (zwarte lijn), terwijl Cy5 op 670 nanometer (rode lijn). In het experiment, Cy3 is gehecht aan CB[7] en Cy5 aan AdA. Tijdens autofagie, de twee kleurstoffen komen dichterbij en Cy3 draagt wat energie over aan zijn nabijgelegen partnerkleurstof Cy5, volgens het FRET-fenomeen. De wetenschappers leggen de ontmoeting van de twee kleurstoffen vast als een toename van de fluorescentie met een golflengte van 644-800 nanometer (blauwe lijn). Krediet:Instituut voor Basiswetenschappen
IBS-wetenschappers van POSTECH bedachten een kwantitatieve procedure om zowel mitochondriën als lysosomen in de loop van de tijd te visualiseren. De relatief eenvoudige en goedkope techniek is nauwkeuriger dan de huidige. Het maakt gebruik van holle tonvormige synthetische moleculen, bekend als cucurbituril (CB[7]), die met uitzonderlijk hoge bindingssterkte bindt aan een molecuul genaamd adamantylamine (AdA) en niet kan worden afgebroken door de lysosomen. CB[7] was versierd met een fluorescerende kleurstof (Cy3), terwijl AdA met een andere kleurstof (Cy5). aanvankelijk, CB[7]-Cy3 komt de lysosomen binnen en Ada-Cy5 de mitochondriën, en dan, wanneer de twee organellen samensmelten in het recyclingproces, CB[7]-Cy3 en Ada-Cy5 binden aan elkaar. Op deze manier, het onderzoeksteam volgde het gedrag van verschillende organellen en observeerde het mitofagieproces in levende cellen. Bovendien, de experimenten toonden aan dat de twee verbindingen niet toxisch zijn voor de cellen onder een dosis van 800 nanomol.
"Het meest uitdagende onderdeel van het experiment was de keuze van de chemicaliën. We kozen chemicaliën met de juiste hydrofiliciteit, opladen, en moleculaire grootte om selectief te worden opgenomen in mitochondriën en lysosomen, " legt PARK Kyeng Min uit, een van de corresponderende auteurs van de studie.
In meer technische termen, de nieuwigheid van dit artikel is afhankelijk van de toepassing van fluorescentieresonantie-energieoverdracht (FRET) op de studie van autofagie. FRET is een afstandsafhankelijke overdracht van energie tussen twee verschillende fluorescerende kleurstoffen; in dit geval Cy3 en Cy5. Als de twee dicht genoeg bij elkaar zijn, Cy3 doneert energie aan Cy5. De wetenschappers leggen de ontmoeting van de twee kleurstoffen vast, aangezien de overdracht van energie van Cy3 naar Cy5 leidt tot een vermindering van de Cy3-fluorescentie-intensiteit ten gunste van een toename van de Cy5-emissie-intensiteit.
In de toekomst, een vergelijkbare techniek zou kunnen worden gebruikt om autofagieprocessen te bestuderen waarbij andere cellulaire organellen betrokken zijn, zoals de eiwitfabrieken Golgi-apparaat en endoplasmatisch reticulum.
 Ultrasone trillingen dwingen een polymeer om een halfgeleider te zijn
Ultrasone trillingen dwingen een polymeer om een halfgeleider te zijn Chemici maken cellulaire krachten zichtbaar op moleculaire schaal
Chemici maken cellulaire krachten zichtbaar op moleculaire schaal Het onderwaterleven belooft wat voor het doden van tuberculose
Het onderwaterleven belooft wat voor het doden van tuberculose Polymeeronderzoekers ontdekken pad naar duurzame en biologisch afbreekbare polyesters
Polymeeronderzoekers ontdekken pad naar duurzame en biologisch afbreekbare polyesters Chemische eigenschappen van benzoëzuur
Chemische eigenschappen van benzoëzuur
Hoofdlijnen
- Onderzoekers ontdekken moleculaire add-ons die eiwitinterfaces aanpassen
- Vissers in Istanbul houden traditie in stand ondanks voorraadalarm
- Herstel van zeezoogdieren aan de westkust verhoogt de consumptie van chinookzalm
- Australische honden getraind om bedreigde diersoorten op te sporen
- Aardworm Kenmerken
- Wat is de chemische samenstelling van de meeste sterren?
- Structuur van het spierstelsel
- Wetenschappers onthullen eiwitstructuur die cruciaal is voor genexpressie
- De rol van microben in de industrie
- Wetenschappers hebben eiwitten gemaakt die worden gecontroleerd door licht
- De energiekloof afstemmen:een nieuwe benadering voor organische halfgeleiders
- Bamboe inspireert tot een optimaal ontwerp voor lichtheid en taaiheid

- Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast

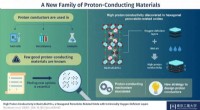
- Nieuwe geleiders met een hoog protonengehalte met inherent zuurstofarme lagen openen een duurzame toekomst
 Aandelen in milieubewuste bedrijven doen het beter dan hun vervuilende concurrenten
Aandelen in milieubewuste bedrijven doen het beter dan hun vervuilende concurrenten Een sfeer van kleur
Een sfeer van kleur Hoe maak je een model van een atoom
Hoe maak je een model van een atoom  Hoe de maximale trekspanning te berekenen
Hoe de maximale trekspanning te berekenen Voedselbezorgers in New York hebben te maken met een schrijnende wereld
Voedselbezorgers in New York hebben te maken met een schrijnende wereld Hoe maak je een krachtige DC elektromagneet
Hoe maak je een krachtige DC elektromagneet  Waarom wisselt een spiegel van links en rechts, maar niet van boven naar beneden?
Waarom wisselt een spiegel van links en rechts, maar niet van boven naar beneden?  Zoeken en redden:onderzoekers op missie om de koraalriffen van Zuid-Florida te redden
Zoeken en redden:onderzoekers op missie om de koraalriffen van Zuid-Florida te redden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

