
Wetenschap
Heeft elke stof een drievoudige punt?
Dit is waarom:
* Definitie van Triple Point: Het drievoudige punt is de specifieke temperatuur en druk waarbij een stof tegelijkertijd in alle drie de fasen kan bestaan:vaste, vloeistof en gas.
* Fasediagrammen: Drievoudige punten worden weergegeven op fasediagrammen. Deze diagrammen tonen de verschillende fasen van een stof als functie van druk en temperatuur.
* stoffen zonder drievoudige punten: Sommige stoffen ontleden of ondergaan chemische reacties voordat ze een punt bereiken waar ze in alle drie de fasen kunnen bestaan. Sommige stoffen kunnen bijvoorbeeld in andere stoffen ontleden voordat ze een drievoudige punt bereiken, of ze kunnen een chemische reactie ondergaan die hun samenstelling volledig verandert.
* Voorbeelden: Stoffen die mogelijk geen drievoudig punt hebben, zijn onder meer:
* Veel organische verbindingen: Ze kunnen ontleden voordat ze hun drievoudige punt bereiken.
* Sommige ionische verbindingen: Ze kunnen chemische reacties ondergaan voordat ze hun drievoudige punt bereiken.
Samenvattend: Hoewel de meeste stoffen een drievoudig punt hebben, zijn er enkele uitzonderingen, vooral voor degenen die vatbaar zijn voor ontleding of chemische reacties onder bepaalde omstandigheden.
 Fiddler op het dak? De noordelijke uitbreiding van het verspreidingsgebied van vioolkrabben kan een teken zijn van klimaatverandering
Fiddler op het dak? De noordelijke uitbreiding van het verspreidingsgebied van vioolkrabben kan een teken zijn van klimaatverandering  Na een bosbrand, attitudes over herstel variëren met gevoel van plaats en overtuigingen over brandecologie
Na een bosbrand, attitudes over herstel variëren met gevoel van plaats en overtuigingen over brandecologie Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?
Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?  Belangrijke inzichten in landdegradatie uit zeven Afrikaanse landen
Belangrijke inzichten in landdegradatie uit zeven Afrikaanse landen Europese wateren zorgen ervoor dat de oceaan omvalt, sleutel voor het reguleren van het klimaat
Europese wateren zorgen ervoor dat de oceaan omvalt, sleutel voor het reguleren van het klimaat
Hoofdlijnen
- De anatomie bepaalt hoe hagedissen partners aantrekken en rivalen afstoten
- Wanneer wordt een mutatie in een DNA-molecuul doorgegeven aan nakomelingen?
- Biologen ontdekken hoe belangrijke mechanismen voor het hechten van koolhydraten niet goed werken
- Lichtshow in levende cellen:nieuwe methode maakt gelijktijdige fluorescerende labeling van veel eiwitten mogelijk
- Wat is fectering?
- Oplossen van hoe een complexe ziekte eiken bedreigt
- Welke microbe is Peneilline?
- Het decoderen van de cognitie van honden:machinaal leren geeft een glimp van hoe de hersenen van een hond weergeven wat hij ziet
- Wat is de evolutie van primaten?
- Herbruikbare stoffen maskers blijven na een jaar wassen goed, drogen

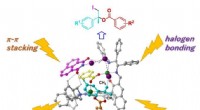
- Asymmetrische joodverestering van eenvoudige alkenen door concerto-katalysator
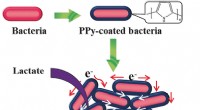
- Geleidende schaal voor bacteriën
- Waterdruppels als geminiaturiseerde reageerbuisjes

- Onderzoeksdoorbraak kan technologie voor schone energie transformeren

 Visualisatie van moleculaire voetballen
Visualisatie van moleculaire voetballen Hoe het ontbrekende getal van het gegeven gemiddelde te vinden
Hoe het ontbrekende getal van het gegeven gemiddelde te vinden  Astronomen identificeren bijna 3, 000 kandidaat-sterren van een nabij stervormend sterrenstelsel
Astronomen identificeren bijna 3, 000 kandidaat-sterren van een nabij stervormend sterrenstelsel Wanneer radioactief fosfor vervalt, zendt het een positron uit. Zal de resulterende kern een andere isotoop van fosfor zijn?
Wanneer radioactief fosfor vervalt, zendt het een positron uit. Zal de resulterende kern een andere isotoop van fosfor zijn?  Retrovirus versus DNA-virus
Retrovirus versus DNA-virus  Ligt er een bondgenoot tegen klimaatverandering onder onze voeten?
Ligt er een bondgenoot tegen klimaatverandering onder onze voeten? Deeltjesfysici werken samen met AI om de moeilijkste wetenschappelijke problemen op te lossen
Deeltjesfysici werken samen met AI om de moeilijkste wetenschappelijke problemen op te lossen Huishoudelijk werk of slapen? Onderzoek zegt dat het ervan afhangt wanneer je geboren bent
Huishoudelijk werk of slapen? Onderzoek zegt dat het ervan afhangt wanneer je geboren bent
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

