
Wetenschap
Lichtshow in levende cellen:nieuwe methode maakt gelijktijdige fluorescerende labeling van veel eiwitten mogelijk
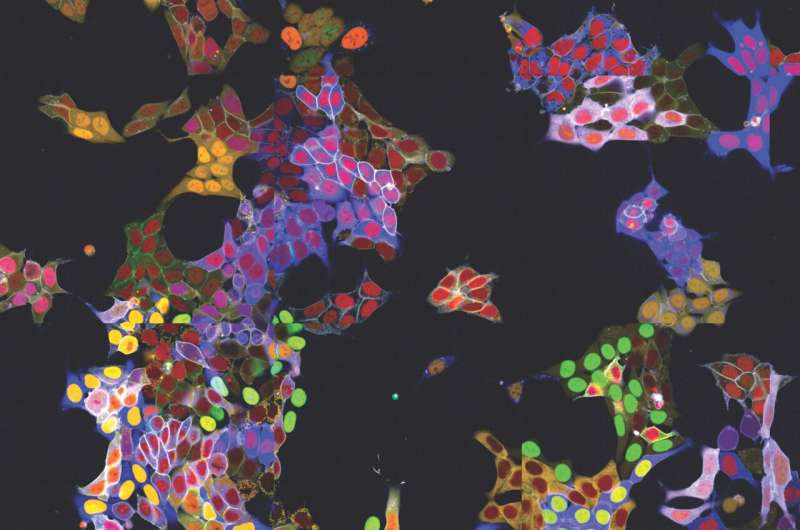
Het nauwkeurig observeren van eiwitten in cellen is uiterst belangrijk voor veel onderzoekstakken, maar is een aanzienlijke technische uitdaging geweest, vooral in levende cellen, omdat de vereiste fluorescerende labeling afzonderlijk aan elk eiwit moest worden bevestigd.
De onderzoeksgroep onder leiding van Stefan Kubicek van CeMM heeft deze hindernis nu overwonnen:met een methode genaamd "vpCells" is het mogelijk om veel eiwitten tegelijkertijd te labelen, met behulp van vijf verschillende fluorescerende kleuren. Deze geautomatiseerde high-throughput-aanpak, geholpen door AI-ondersteunde beeldherkenning, opent geheel nieuwe toepassingen in verschillende disciplines, van fundamentele celbiologie tot de ontdekking van geneesmiddelen. De studie is gepubliceerd in het tijdschrift Nature Cell Biology .
Zonder eiwitten zou het leven zoals wij dat kennen ondenkbaar zijn. Ze vormen het structurele raamwerk voor cellen, fungeren als enzymen om het metabolisme te controleren en stellen cellen in staat te communiceren met hun omgeving als membraanreceptoren, transporteurs of signaalmoleculen. Al deze functies kunnen alleen worden vervuld als de eiwitten zich op de juiste plek in de cel bevinden. Vaak veranderen zelfs de eigenschappen van een eiwit als het van locatie verandert. Controle over de lokalisatie in de cel betekent dus ook controle over zijn functie.
Om de functie van eiwitten te begrijpen en te onderzoeken, is het essentieel om hun locatie in de cel nauwkeurig te bepalen en te volgen. Eiwitten pendelen vaak dynamisch tussen verschillende organellen en compartimenten van de cel. Om ze onder de microscoop zichtbaar te maken, worden ze vaak gekoppeld aan een fluorescerende, helder glanzende eiwitcomponent. Deze methode stuitte echter op technische problemen:doorgaans kon de fluorescerende component slechts aan één eiwit tegelijk worden vastgemaakt, en om meerdere eiwitten te labelen moesten cellen meestal worden gedood en gefixeerd.
De nieuwe methode gepresenteerd door de groep van Stefan Kubicek, genaamd "visual proteomics Cells" (afgekort vpCells), maakt het mogelijk dat eiwitten fluorescent worden gelabeld op een manier die hun endogene regulerende mechanismen behoudt. In plaats van één eiwit tegelijk te labelen, kunnen vpCells veel eiwitten tegelijkertijd fuseren met een fluorescerende tag in een zogenaamde multiplex-aanpak.
Een voorloper van deze methode werd in 2020 al door het team van Kubicek beschreven voor het bestuderen van metabolische enzymen. Nu is het op drie manieren uitgebreid en verbeterd:
Ten eerste kunnen vpCells alle theoretisch mogelijke eiwitten labelen met behulp van de CRISPR/Cas9-genbewerkingstool om fluorescerende eiwitten genetisch aan de onderzochte eiwitten te hechten. De groep van Kubicek heeft voor dit doel een genoombrede "bibliotheek" gecreëerd, die de fluorescerende markering en systematische functionele verkenning van alle mogelijke menselijke eiwitten mogelijk maakt.
Ten tweede gebruiken vpCells niet slechts één fluorescerende kleur, maar in totaal vijf complementaire kleuren. In elke cel worden twee verschillende te volgen eiwitten gemarkeerd. Bovendien wordt een andere kleurmarkering gebruikt om individuele klonen beter te onderscheiden. En nog twee kleuren markeren de celkern en het membraan om individuele cellen beter af te bakenen.
Ten derde maakt dit kleurenschema het niet alleen mogelijk om visueel aantrekkelijke beelden te genereren, maar ook om de verschillende eiwitten optisch te herkennen en te onderscheiden. Normaal gesproken vereist dit complexe DNA-sequencing na beeldvorming om te bepalen welk eiwit is gelabeld. De vpCells-aanpak maakt het daarentegen mogelijk om een AI-ondersteund beeldherkenningssysteem te trainen om te herkennen welk eiwit in welke cel is gemarkeerd, uitsluitend op basis van fluorescentiemicroscopiebeelden.
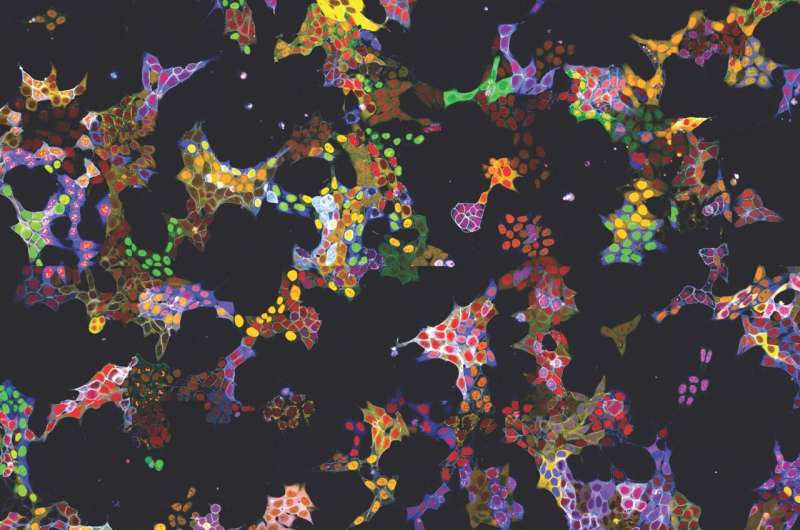
De methode heeft zijn nut al in twee toepassingen aangetoond:enerzijds werden meer dan 4.500 cellijnen gegenereerd als reporters voor meer dan 1.100 eiwitten. Deze cellijnen werden gebruikt om de AI-modellen te trainen en om de lokalisatie van de eiwitten in hun basale toestand te beschrijven. Alle afbeeldingen van de individueel gelabelde eiwitten zijn beschikbaar in de publiekelijk toegankelijke webdatabase vpCells.
Aan de andere kant werden de levende reportercellen gebruikt voor een specifieke onderzoeksvraag:het team van Kubicek onderzocht het effect van ruim 1000 kleine molecuulstoffen op 61 voor kankercellen relevante eiwitten. De onderzoekers ontdekten dat 44 van de geteste stoffen binnen zes uur de hoeveelheid of lokalisatie van individuele eiwitten veranderden. Eén van de stoffen bleek een remmer te zijn van het eiwittransport vanuit de celkern, wat een vergelijkbare werking heeft als een klinisch goedgekeurd medicijn tegen multipel myeloom, een kanker van het bloedvormende systeem.
"Deze resultaten bieden een eerste glimp van de veelzijdigheid van de vpCells-methode", zegt Kubicek. "We verwachten nog veel meer toekomstige toepassingen, van fundamentele celbiologie tot toegepaste medicijnontdekking."