
Wetenschap
Waarom is natrium een metaal?
1. Chemische eigenschappen :Natriumatomen verliezen gemakkelijk één elektron uit hun buitenste schil om een stabiele elektronenconfiguratie te bereiken. Dit vermogen om gemakkelijk een elektron af te staan, maakt natrium zeer elektropositief en reactief, wat karakteristieke eigenschappen van metalen zijn.
2. Elektronenconfiguratie :Het atoomnummer van natrium is 11, wat betekent dat het 11 protonen en 11 elektronen heeft. De elektronische configuratie van natrium kan worden weergegeven als 2, 8, 1. De buitenste schil (n =1) heeft slechts één elektron, dat losjes aan de kern is gebonden. Dit enkele losjes vastgehouden elektron wordt een valentie-elektron genoemd.
3. Glanzend uiterlijk :Zoals de meeste metalen heeft natrium een glanzend of glanzend uiterlijk. Dit komt door de aanwezigheid van vrije mobiele valentie-elektronen die vrij kunnen bewegen en licht kunnen reflecteren, waardoor natrium een metaalachtige glans krijgt.
4. Hoge elektrische geleidbaarheid :Natrium is een uitstekende geleider van elektriciteit. Wanneer een elektrisch veld wordt aangelegd, kunnen de vrije valentie-elektronen in natrium vrij door het metaal bewegen en de elektrische stroom geleiden. Deze hoge elektrische geleidbaarheid is een kenmerkende eigenschap van metalen.
5. Hoge thermische geleidbaarheid :Natrium is ook een goede warmtegeleider. De vrij bewegende valentie-elektronen in natrium kunnen thermische energie efficiënt overbrengen, waardoor warmte snel door het metaal kan stromen.
6. Moeibaarheid en taaiheid :Natrium is een zacht, kneedbaar metaal dat gemakkelijk kan worden gevormd door hameren of walsen. Het is ook taai, wat betekent dat het tot dunne draden kan worden getrokken zonder te breken. Deze eigenschappen zijn typerend voor metalen elementen.
7. Reactiviteit :Natrium is zeer reactief, vooral met water. Wanneer natrium in contact komt met water, ondergaat het een krachtige chemische reactie, waarbij waterstofgas vrijkomt en natriumhydroxide (NaOH) ontstaat. Deze reactiviteit is te wijten aan de lage ionisatie-energie van natrium en de sterke neiging ervan om zijn valentie-elektron te verliezen.
De combinatie van deze eigenschappen, waaronder de chemische aard, elektronenconfiguratie, glanzend uiterlijk, elektrische geleidbaarheid, thermische geleidbaarheid, kneedbaarheid, ductiliteit en reactiviteit, geeft duidelijk aan dat natrium inderdaad een metaal is.
 Hoe zijn de aarde en de zon gelijk of verschillend?
Hoe zijn de aarde en de zon gelijk of verschillend?  State-of-the-art klimaatmodel laat zien hoe we een crisis kunnen oplossen
State-of-the-art klimaatmodel laat zien hoe we een crisis kunnen oplossen Negen doden door tyfoon die Zuid-Korea teistert
Negen doden door tyfoon die Zuid-Korea teistert Olie- en aardgasproductie stoot meer methaan uit dan eerder werd gedacht
Olie- en aardgasproductie stoot meer methaan uit dan eerder werd gedacht Uit onderzoek blijkt dat meer dan de helft van het water uit de Colorado Rivers wordt gebruikt om gewassen te irrigeren
Uit onderzoek blijkt dat meer dan de helft van het water uit de Colorado Rivers wordt gebruikt om gewassen te irrigeren
Hoofdlijnen
- De gemiddelde levensduur van skeletspiercellen
- Roofzuchtige bacteriën gevonden in studie van longmicrobioom van patiënten met cystische fibrose
- Cellulaire route zou bewijs kunnen leveren van hoe kanker en obesitas met elkaar verbonden zijn
- Hoe de vogels en de bijen koffieplanten helpen
- Wat is een FLASK-definitie?
- Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten
- Studie wijst op cellulaire respons op druk in zeester-embryo's
- Wat is de belangrijkste functie van de hersenen?
- Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen
- Chemische ingenieurs ontwikkelen nieuwe klasse multifunctioneel precisiepolymeer

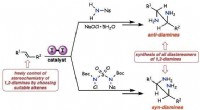
- Moleculair jodium katalyseert processen voor antivirale en farmaceutische syntheses
- Enorm potentieel voor elektronisch textiel gemaakt met nieuwe cellulosedraad

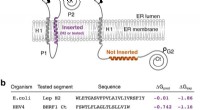
- Onderzoek toont de rol aan van intra-mebrane interacties bij de beheersing van celdood door virussen
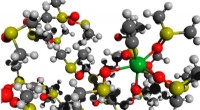
- Een nieuwe strategie voor een groener gebruik van calciumcarbide
 Wetenschappers tonen aan dat positief geladen hydrogels de overleving en groei van neurale stamcellen bevorderen
Wetenschappers tonen aan dat positief geladen hydrogels de overleving en groei van neurale stamcellen bevorderen  Bacteriële biofilms gebruiken voor de productie van nieuwe zelfherstellende materialen en bioprocessing-technologieën
Bacteriële biofilms gebruiken voor de productie van nieuwe zelfherstellende materialen en bioprocessing-technologieën Tekenen en symptomen van hondsdolheid bij eekhoorns
Tekenen en symptomen van hondsdolheid bij eekhoorns De meeste ionische verbindingen bestaan uit een?
De meeste ionische verbindingen bestaan uit een?  Hoe cellen fouten corrigeren onder tijdsdruk
Hoe cellen fouten corrigeren onder tijdsdruk NASA-ruimtevaartuig schiet naar de zon om het nog beter te kunnen zien
NASA-ruimtevaartuig schiet naar de zon om het nog beter te kunnen zien Welk wetenschappelijk instrument wordt gebruikt om licht te verzamelen door middel van een camera?
Welk wetenschappelijk instrument wordt gebruikt om licht te verzamelen door middel van een camera?  Welke dieren leven er op de bosbodem?
Welke dieren leven er op de bosbodem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

