
Wetenschap
Hoeveel joule warmte is nodig om 24,40 gram water op het kookpunt volledig te verdampen?
De verdampingsenthalpie van water is 40,79 kJ/mol. Dit betekent dat er 40,79 kJ energie nodig is om één mol water te verdampen.
We kunnen deze informatie gebruiken om de hoeveelheid warmte te berekenen die nodig is om 24,40 gram water te verdampen. Eerst moeten we het aantal mol water in 24,40 gram berekenen:
$$24,40 \text{ g H}_2\text{O} \times \frac{1 \text{ mol H}_2\text{O}}{18,02 \text{ g H}_2\text{O}} =1,354 \text{ mol H}_2\text{O}$$
Vervolgens kunnen we de verdampingsenthalpie gebruiken om de hoeveelheid warmte te berekenen die nodig is om deze hoeveelheid water te verdampen:
$$1,354 \text{ mol H}_2\text{O} \times 40,79 \text{ kJ/mol} =55,14 \text{ kJ}$$
Daarom is er 55,14 kJ warmte nodig om 24,40 gram water bij het kookpunt volledig te verdampen.
 Een nieuwe kijk op onderwaterbeelden
Een nieuwe kijk op onderwaterbeelden Hoe hybride plantenvariëteiten de uitdagingen van voedselzekerheid en klimaatverandering kunnen aanpakken
Hoe hybride plantenvariëteiten de uitdagingen van voedselzekerheid en klimaatverandering kunnen aanpakken  Meer redenen voor optimisme over klimaatverandering dan we in decennia hebben gezien
Meer redenen voor optimisme over klimaatverandering dan we in decennia hebben gezien Houstons post-Harvey giftige puinhoop
Houstons post-Harvey giftige puinhoop Gevaarlijke orkaan Willa onderzocht door NASA en de Japanse GPM-satelliet
Gevaarlijke orkaan Willa onderzocht door NASA en de Japanse GPM-satelliet
Hoofdlijnen
- Wat is divergentie in de evolutie?
- Hoe de varkensgriep werkt
- Onderzoekers ontdekken hoe vogelveren bestand zijn tegen scheuren
- Verschillen tussen een neuron en een neuroglia
- 8 supercoole genetische mutaties gevonden bij mensen
- Opnieuw klonen van de eerste gekloonde hond die tot nu toe als succesvol werd beschouwd
- Enzymen kunnen de sleutel zijn om te begrijpen hoe DNA muteert, vinden kwantumbiologen
- Wat sprinkhanen eten
- Kunnen scholen vissen worden geïdentificeerd zonder menselijke tussenkomst?
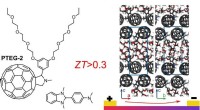
- Warmte omzetten in kracht met efficiënt organisch thermo-elektrisch materiaal
- Magnetrons tegen koude start-emissies

- Wetenschappers onderzoeken macrocyclische peptiden als nieuwe medicijnsjablonen

- Onderzoeksteam ontwikkelt nieuwe klasse zachte materialen

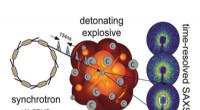
- Eerste Amerikaanse experimenten ooit in nieuwe röntgenfaciliteit kunnen leiden tot betere modellering van explosieven
 Hoe Density of Sphere te berekenen
Hoe Density of Sphere te berekenen Waarom zijn we zo verdeeld? Nulsomdenken is daar een onderdeel van
Waarom zijn we zo verdeeld? Nulsomdenken is daar een onderdeel van  NASA voert veldtest uit van 3D-beeldvormingssysteem voor afdaling en landing
NASA voert veldtest uit van 3D-beeldvormingssysteem voor afdaling en landing Kan overtollig water uit olie- en gasactiviteiten boeren helpen de seismiciteit te verminderen?
Kan overtollig water uit olie- en gasactiviteiten boeren helpen de seismiciteit te verminderen?  Hoe versterkers op gelijkstroommotoren te controleren
Hoe versterkers op gelijkstroommotoren te controleren Wiskundige regels voor aftrekken
Wiskundige regels voor aftrekken  Nieuwe analytische technologie onthult nanomechanische oppervlaktekenmerken
Nieuwe analytische technologie onthult nanomechanische oppervlaktekenmerken Hoe voorspellers orkaan Dorian volgen
Hoe voorspellers orkaan Dorian volgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

