
Wetenschap
Bepaal de reactiewarmte voor deze chemische reacties. Zijn ze endo- of exotherm 1. C s H 2 O g CO 2. Het lijkt erop dat ik niet twee keer hetzelfde antwoord krijg. Kan iemand mij helpen?
1.
>Verbranding van methaan:
```
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
```
Enthalpieverandering: ΔH =-890 kJ/mol
Deze reactie is exotherm omdat het warmte afgeeft aan de omgeving.
---
2.
>Ontbinding van water:
```
2H₂O(l) → 2H₂(g) + O₂(g)
```
Enthalpieverandering: ΔH =+286 kJ/mol
Deze reactie is endotherm omdat het warmte uit de omgeving absorbeert.
 Ionen in gesmolten zouten kunnen tegen de stroom in gaan
Ionen in gesmolten zouten kunnen tegen de stroom in gaan Wat is de uitgebalanceerde chemische vergelijking voor een verbrande kaars?
Wat is de uitgebalanceerde chemische vergelijking voor een verbrande kaars?  Nieuwe methode maakt gemakkelijke, veelzijdige synthese van lactonmoleculen mogelijk
Nieuwe methode maakt gemakkelijke, veelzijdige synthese van lactonmoleculen mogelijk Magnesiumsulfaat plus natriumcarbonaat is gelijk aan?
Magnesiumsulfaat plus natriumcarbonaat is gelijk aan?  Team onthult eenvoudige methode om hoogwaardige lithium-seleniumbatterijen te produceren
Team onthult eenvoudige methode om hoogwaardige lithium-seleniumbatterijen te produceren
 Wat betekent Earth Day als mensen planeetvormende krachten bezitten?
Wat betekent Earth Day als mensen planeetvormende krachten bezitten? Verschillen tussen rivierkreeften en sprinkhanen
Verschillen tussen rivierkreeften en sprinkhanen  Wetenschappers ontdekken hoe 's werelds grootste vulkanen zijn ontstaan
Wetenschappers ontdekken hoe 's werelds grootste vulkanen zijn ontstaan Het klimaatverleden van Yucatan informeert het huidige mondiale klimaat
Het klimaatverleden van Yucatan informeert het huidige mondiale klimaat NASA vindt tropische depressie 23Ws sterkste stormen in twee landen
NASA vindt tropische depressie 23Ws sterkste stormen in twee landen
Hoofdlijnen
- Hoe een Antarctische worm antivries maakt en wat dat met klimaatverandering te maken heeft
- Onderzoeker bespreekt de biologische overspraak tussen microben en gastheren
- Oorsprong van het leven? Ontdekking zou kunnen helpen verklaren hoe de eerste organismen op aarde ontstonden
- Een probioticum voor onze longen? Nieuw onderzoek roept vragen op over de toekomst van de behandeling van COVID-19
- Wat is de rol van natuurlijke selectie in convergente evolutie?
- Wordt de nucleaire envelop aangetroffen in een plantencel of een dierlijke cel?
- Waarom zijn archaea en bacteriën anders dan andere koninkrijken?
- Polygene eigenschappen: definitie, voorbeeld en feiten
- Onderzoek laat zien hoe planten de ‘herinnering’ aan een hoog kooldioxidegehalte doorgeven aan hun nakomelingen
- Nieuwe proteomics-techniek geeft inzicht in ubiquitine-signalering

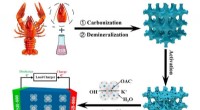
- Afval om te koesteren:Rivierkreeftschelpen om energie op te slaan
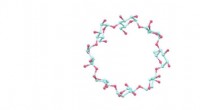
- Dit molecuul is gemaakt van suiker, in de vorm van een donut, en gevormd met behulp van licht
- Meer MXene maken:onderzoekers onthullen een schaalbaar productiesysteem voor de veelbelovende, 2-D nanomaterialen

- Waarom sommige groenen bruin worden in historische schilderijen

 Wat zijn de voordelen van de transmissie-elektronenmicroscoop?
Wat zijn de voordelen van de transmissie-elektronenmicroscoop?  Weten apen wanneer ze moeten 'googlen'?
Weten apen wanneer ze moeten 'googlen'?  Griekenland racet om het elektriciteitsnet te herstellen nu de koudegolf afneemt
Griekenland racet om het elektriciteitsnet te herstellen nu de koudegolf afneemt Scheve vissen laten zien dat symmetrie slechts oppervlakkig is
Scheve vissen laten zien dat symmetrie slechts oppervlakkig is  Zelfbeheersing en keuzes:waarom we de gemakkelijke weg kiezen nadat we ons hebben ingespannen
Zelfbeheersing en keuzes:waarom we de gemakkelijke weg kiezen nadat we ons hebben ingespannen  Hoe het aantal overtollige elektronen te vinden
Hoe het aantal overtollige elektronen te vinden Hoe klimaatverandering de seizoenen beïnvloedt
Hoe klimaatverandering de seizoenen beïnvloedt  Astronaut Michael Collins, Apollo 11 piloot, dood aan kanker
Astronaut Michael Collins, Apollo 11 piloot, dood aan kanker
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

