
Wetenschap
Wat leidt tot de toename van de snelheid van een chemische reactie?
1. Temperatuur:Naarmate de temperatuur stijgt, neemt de gemiddelde kinetische energie van de reactantmoleculen toe. Dit betekent dat ze sneller bewegen en vaker en met meer energie met elkaar in botsing komen, waardoor de kans op een succesvolle reactie groter wordt.
2. Concentratie:Het verhogen van de concentratie van de reactanten betekent dat er meer reactantmoleculen aanwezig zijn in een bepaald volume. Dit vergroot de kans op botsingen tussen reactantmoleculen en bijgevolg de reactiesnelheid.
3. Oppervlakte:Door het oppervlak van vaste of vloeibare reactanten te vergroten, vergroot het aantal deeltjes dat aan elkaar wordt blootgesteld en beschikbaar is voor reactie. Dit kan de reactiesnelheid aanzienlijk versnellen.
4. Katalysator:Een katalysator is een stof die een chemische reactie versnelt zonder daarbij te worden verbruikt. Katalysatoren verlagen de activeringsenergie van de reactie, waardoor het voor reactanten gemakkelijker wordt om de overgangstoestand te bereiken en producten te vormen.
5. Licht:Bij fotochemische reacties wordt lichtenergie geabsorbeerd door reactantmoleculen, waardoor ze in een aangeslagen toestand terechtkomen. Deze aangeslagen moleculen zijn reactiever en kunnen gemakkelijker reacties ondergaan, waardoor de reactiesnelheid toeneemt.
6. Druk:Bij reacties waarbij gassen betrokken zijn, kan het verhogen van de druk de reactiesnelheid verhogen door meer reactantmoleculen dichter bij elkaar te dwingen en de frequentie van botsingen te vergroten.
7. Enzymen:Bij biochemische reacties fungeren enzymen als katalysatoren om de snelheid van specifieke reacties te versnellen. Ze binden zich aan de reactanten, vormen een enzym-substraatcomplex en verlagen de activeringsenergie die nodig is om de reactie te laten plaatsvinden.
8. Ionische kracht:Bij reacties waarbij ionen in de oplossing betrokken zijn, kan het verhogen van de ionensterkte van de oplossing de reactiesnelheid beïnvloeden door de activiteit en interacties van de ionen te beïnvloeden.
Het is belangrijk op te merken dat deze factoren verschillende effecten kunnen hebben op verschillende reacties, en dat de specifieke impact afhangt van de aard van de reactie en de omstandigheden waaronder deze plaatsvindt.
 Superhydrofobe magnetische spons om water uit olieproducten te helpen zuiveren
Superhydrofobe magnetische spons om water uit olieproducten te helpen zuiveren Studie onthult de mechanismen van een eiwit dat mos en groene algen helpt zich te verdedigen tegen te veel licht
Studie onthult de mechanismen van een eiwit dat mos en groene algen helpt zich te verdedigen tegen te veel licht Nieuwe membranen helpen de CO2-uitstoot te verminderen
Nieuwe membranen helpen de CO2-uitstoot te verminderen Nieuwe techniek om supersponzen te maken is een game changer
Nieuwe techniek om supersponzen te maken is een game changer Lief hoor! Met suiker beklede sonde levert betere zuurtest op
Lief hoor! Met suiker beklede sonde levert betere zuurtest op
 Klimaatverandering kan meer sediment en vervuiling opleveren voor de San Francisco Bay-Delta
Klimaatverandering kan meer sediment en vervuiling opleveren voor de San Francisco Bay-Delta Wat gebeurt er met onze opdrogende riviernetwerken? Een nieuwe app helpt wetenschappers erachter te komen
Wat gebeurt er met onze opdrogende riviernetwerken? Een nieuwe app helpt wetenschappers erachter te komen Koolstofafgevende zombiebranden in veengebieden kunnen worden gedempt door nieuwe bevindingen
Koolstofafgevende zombiebranden in veengebieden kunnen worden gedempt door nieuwe bevindingen Klimaatverandering vereist hetzelfde leiderschap als COVID-19, en Australië faalt
Klimaatverandering vereist hetzelfde leiderschap als COVID-19, en Australië faalt Geotextiel kan het smelten van gletsjers vertragen, maar tegen welke prijs?
Geotextiel kan het smelten van gletsjers vertragen, maar tegen welke prijs?
Hoofdlijnen
- Teams Advance maakt het bewerken van genen met chirurgische precisie mogelijk
- Nieuw onderzoek laat zien hoe genen aan en uit gaan
- Waarom wiebelen planten? Nieuw onderzoek biedt antwoorden
- Hoe heeft Barbara McClintock een belangrijke bijdrage geleverd aan de studie van de genetica?
- Onderzoekers identificeren hoe de bacteriële replicatieve helicase zich opent om het DNA-replicatieproces te starten
- Hoe extrusie van epitheelcellen wordt gereguleerd door dichtheid
- Onderzoekers onthullen nieuwe inzichten in de controle van cellulaire steigers
- Waarom beschouwen wetenschappers virussen als niet-levend?
- Hoe ontwikkelen Candida auris en andere schimmels resistentie tegen geneesmiddelen? Een microbioloog legt het uit
- Nieuw glow-in-the-dark materiaal kan pad van drugs door het menselijk lichaam volgen

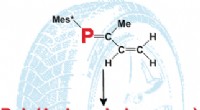
- Een chemisch functionele fosforversie van natuurlijk rubber
- Een ontbrekende schakel van methaan naar methanol blootleggen

- Sporen van opiaten gevonden in oud Cypriotisch schip

- Een nieuw soort vaccin op basis van spinrag
 Seashell-feiten voor kinderen
Seashell-feiten voor kinderen Nieuwe inzichten over de rol van vakbonden in de strijd voor rechten
Nieuwe inzichten over de rol van vakbonden in de strijd voor rechten Polarisatie van nieuws over klimaatverandering is geen hoax
Polarisatie van nieuws over klimaatverandering is geen hoax Halfgeleiders van eigen bodem voor snellere, kleinere elektronica
Halfgeleiders van eigen bodem voor snellere, kleinere elektronica Als iedereen op afstand werkt, communicatie en samenwerking lijden, studie vondsten
Als iedereen op afstand werkt, communicatie en samenwerking lijden, studie vondsten Google Assistent om webpagina's hardop voor te lezen op sommige apparaten
Google Assistent om webpagina's hardop voor te lezen op sommige apparaten Hoeveel atomen zitten er in één molecuul antivries?
Hoeveel atomen zitten er in één molecuul antivries?  Kinderen verdienen antwoorden op hun vragen over klimaatverandering:hoe universiteiten kunnen helpen
Kinderen verdienen antwoorden op hun vragen over klimaatverandering:hoe universiteiten kunnen helpen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

