
Wetenschap
Waarom reageert quinuclidine sneller dan triethylamine met isopropylchloride in een SN2-reactie?
1. Nucleofiliciteit: Quinuclidine is een sterker nucleofiel dan triethylamine. Dit komt omdat het stikstofatoom in chinuclidine basischer is dan het stikstofatoom in triethylamine. Hoe basischer het stikstofatoom, hoe gemakkelijker het een paar elektronen kan doneren om een nieuwe binding te vormen.
2. Sterische hinder: Triethylamine is een omvangrijker molecuul dan quinuclidine. Dit betekent dat de drie ethylgroepen in triethylamine meer sterische hinder creëren rond het stikstofatoom, waardoor het voor het stikstofatoom moeilijker wordt om te reageren met het isopropylchloride. Quinuclidine daarentegen is een kleiner molecuul met minder sterische hinder, waardoor het stikstofatoom gemakkelijker kan reageren met het isopropylchloride.
3. Oplosmiddeleffecten: De reactie tussen chinuclidine en isopropylchloride wordt doorgaans uitgevoerd in een polair aprotisch oplosmiddel, zoals dimethylformamide (DMF). DMF is een goed oplosmiddel voor deze reactie omdat het zowel het nucleofiel als het elektrofiel kan solvateren en de reactie niet verstoort. Triethylamine daarentegen is een slechte nucleofiel in polaire aprotische oplosmiddelen. Dit komt omdat de polaire aprotische oplosmiddelmoleculen concurreren met het triethylamine om het isopropylchloride, wat de concentratie van het triethylamine-isopropylchloridecomplex vermindert en de reactie vertraagt.
Samenvattend reageert quinuclidine sneller dan triethylamine met isopropylchloride in een SN2-reactie omdat het een sterkere nucleofiel is, minder sterische hinder heeft en beter oplosbaar is in het reactieoplosmiddel.
 Frankrijk zet zich schrap voor hevige stormen na wekenlange droogte
Frankrijk zet zich schrap voor hevige stormen na wekenlange droogte Vissende nomaden:karpers bijeendrijven op het Thousand Island-meer in China
Vissende nomaden:karpers bijeendrijven op het Thousand Island-meer in China Factoren die weer en klimaat beïnvloeden
Factoren die weer en klimaat beïnvloeden NASA-satellietbeelden vinden Rebekah nu post-tropisch
NASA-satellietbeelden vinden Rebekah nu post-tropisch De schaaldieren ter wereld worden bedreigd naarmate onze oceanen zuurder worden
De schaaldieren ter wereld worden bedreigd naarmate onze oceanen zuurder worden
Hoofdlijnen
- Bestaat er een geloofwaardige wetenschappelijke theorie die evolutie tegenspreekt?
- Beschrijving van de basisfuncties van enzymen in cellen
- Hoe vleermuishersenen luisteren naar binnenkomende signalen tijdens echolocatie
- Waar komt de kleur vandaan in paarse kool?
- Dance-gerelateerde wetenschapsprojecten
- Wat is het verschil tussen dierlijke cellen en plantencellen?
- Verschillen in mannelijke en vrouwelijke chromosomen
- Hoe nemen we beslissingen?
- Nieuwe screeningstechniek stelt veredelaars in staat sneller droogteresistente rassen te ontwikkelen
- De ontdekking van vloeibaar metaal luidt een nieuwe golf van chemie en elektronica in

- Deze hydrogeltablet kan een liter rivierwater in een uur zuiveren

- Onderzoekers kunnen rekenen op verbeterde proteomics-methode

- Strategie suggereert manieren om zich voor te bereiden op opkomende antibioticaresistente superbacteriën

- Nieuwsgierige in elkaar grijpende moleculen vertonen een dubbele respons
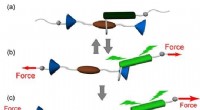
 Onderzoekers rapporteren een fundamentele spiersnelheidslimiet
Onderzoekers rapporteren een fundamentele spiersnelheidslimiet Onderzoeker bespreekt programma's voor het delen van fietsen
Onderzoeker bespreekt programma's voor het delen van fietsen NASA ziet de spiraal in tyfoon Cimaron
NASA ziet de spiraal in tyfoon Cimaron Hoe overheidsbeleidsmakers gegevens uit nieuw onderzoek kunnen gebruiken om klimaatdoelen te bereiken
Hoe overheidsbeleidsmakers gegevens uit nieuw onderzoek kunnen gebruiken om klimaatdoelen te bereiken  Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen?
Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen? Nieuwe materialen kunnen de prestaties van perovskiet-zonnecellen helpen verbeteren
Nieuwe materialen kunnen de prestaties van perovskiet-zonnecellen helpen verbeteren Particulier Amerikaans ruimtevaartuig komt in een baan rond de maan, voorafgaand aan de landingspoging
Particulier Amerikaans ruimtevaartuig komt in een baan rond de maan, voorafgaand aan de landingspoging  Soorten titratie
Soorten titratie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

