
Wetenschap
Hoeveel niet-bindende elektronen zitten er in een watermolecuul?
Er zijn vier paren niet-bindende elektronen in een watermolecuul.
Twee van deze paren niet-bindende elektronen zijn geassocieerd met het zuurstofatoom, dat zes valentie-elektronen heeft. Vier van deze elektronen worden gebruikt om covalente bindingen te vormen met de twee waterstofatomen, waardoor er twee niet-bindende elektronen overblijven. De andere twee paren niet-bindende elektronen zijn geassocieerd met de twee waterstofatomen, die elk één valentie-elektron hebben. Dit elektron vormt een covalente binding met het zuurstofatoom, waardoor er één niet-bindend elektron overblijft.
 De kracht van planten en hoe ze de manier waarop we leven veranderen
De kracht van planten en hoe ze de manier waarop we leven veranderen  Overstromingen in het stroomgebied van de Columbia-rivier zullen naar verwachting toenemen onder klimaatverandering
Overstromingen in het stroomgebied van de Columbia-rivier zullen naar verwachting toenemen onder klimaatverandering Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen?
Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen? Hoe groot kan een rat krijgen?
Hoe groot kan een rat krijgen?  Studie brengt overvloed aan plastic afval in Europese en Aziatische rivieren in kaart
Studie brengt overvloed aan plastic afval in Europese en Aziatische rivieren in kaart
Hoofdlijnen
- Journal beschrijft hoe de opwarming van de aarde de visserij in de wereld zal beïnvloeden
- Sommige planten worden groter - en gemener - als ze worden geknipt, studie vondsten
- Schimmelparing:volgend wapen tegen maïsaflatoxine?
- Welk deel van de plant is verantwoordelijk voor het verkrijgen van water bij de meeste planten?
- Moeten we de natuur beschermen omwille van zichzelf? Voor zijn economische waarde? Omdat het ons gelukkig maakt? Ja
- Waarom wordt een microscoop samengestelde microscoop genoemd?
- Waarom zijn de Neanderthalers uitgestorven?
- Welke enzymen verteren koolhydraten?
- Onderzoekers richten zich op de productie van spermidine om de opkomende medicijnresistentie bij Salmonella te bestrijden
- Een zelfherstellend composiet

- Verdrievoudiging van de efficiëntie van op zonne-energie gebaseerde waterstofbrandstofopwekking met metalen nanostructuren die licht vertragen

- Directe elektrolyse heeft gemengde resultaten voor het extraheren van brandstofbronnen uit microalgen

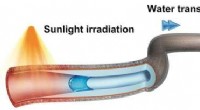
- Snel gecontroleerd transport van waterdruppels door door zonlicht aangedreven pomp
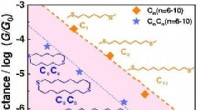
- Zeer isolerende alkaanringen met destructieve σ-interferentie
 Wat ligt er onder de andere kant van de maan?
Wat ligt er onder de andere kant van de maan?  Waarom blijft ijs aan je vingers plakken?
Waarom blijft ijs aan je vingers plakken?  Machine learning in de landbouw:wetenschappers leren computers om stress bij soja te diagnosticeren
Machine learning in de landbouw:wetenschappers leren computers om stress bij soja te diagnosticeren Een nieuwe bètavoltaïsche technologie met kleurstoffen voor een betere energieproductie
Een nieuwe bètavoltaïsche technologie met kleurstoffen voor een betere energieproductie Onderzoekers onderzoeken voordelen van grazende schapen in de groenteteelt
Onderzoekers onderzoeken voordelen van grazende schapen in de groenteteelt Personen met een strafblad kunnen langer in hun baan blijven
Personen met een strafblad kunnen langer in hun baan blijven Berekening van de prijselasticiteit van de vraag
Berekening van de prijselasticiteit van de vraag Heeft zilver een verschillende zuiverheid, dat wil zeggen karaat?
Heeft zilver een verschillende zuiverheid, dat wil zeggen karaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

