
Wetenschap
Waarom wordt zwavel in chemische vergelijkingen geschreven als S en niet als S8?
1. Eenvoudiger weergave:In chemische vergelijkingen ligt de nadruk op de reactie en transformaties tussen verschillende elementen en verbindingen. Het gebruik van het symbool S in plaats van S8 vereenvoudigt de notatie, waardoor vergelijkingen gemakkelijker te lezen en te begrijpen zijn.
2. Generalisatie van reacties:Chemische vergelijkingen zijn bedoeld om de algehele transformatie van reactanten in producten weer te geven. Door S te gebruiken, wordt het toepasbaar op verschillende vormen van zwavel, zoals elementaire zwavel (S8), sulfide-ionen (S2-) of andere zwavelhoudende soorten, zonder een bepaalde moleculaire vorm te specificeren.
3. Stoichiometrische overwegingen:Bij stoichiometrische berekeningen en het balanceren van chemische vergelijkingen maakt het gebruik van S een meer algemene weergave mogelijk van de hoeveelheid zwavel die bij de reactie betrokken is. Als bij een reactie bijvoorbeeld 2 mol elementaire zwavel betrokken is, kan deze worden weergegeven als 2S, in plaats van expliciet 2S8 te vermelden.
4. Thermodynamische en evenwichtsstudies:Bij thermodynamische berekeningen en evenwichtsstudies vereenvoudigt het gebruik van S in plaats van S8 de analyse en wiskundige behandeling. Het maakt de beschouwing van verschillende zwavelsoorten en hun bijdragen mogelijk zonder zich te verdiepen in specifieke moleculaire structuren.
5. Algemene praktijk:De conventie om S te gebruiken om zwavel weer te geven in chemische vergelijkingen wordt algemeen aanvaard in de wetenschappelijke gemeenschap en wordt al vele jaren consequent toegepast in schoolboeken, wetenschappelijke literatuur en onderzoeksartikelen.
 Doodt waterstofperoxide bacteriën?
Doodt waterstofperoxide bacteriën?  Waarom wordt het vaseline genoemd als het gemaakt is met vaseline en niet met wat olie?
Waarom wordt het vaseline genoemd als het gemaakt is met vaseline en niet met wat olie?  Natuurlijke stoffen zijn veelbelovend tegen het coronavirus
Natuurlijke stoffen zijn veelbelovend tegen het coronavirus Wat maakt binding tussen metalen mogelijk?
Wat maakt binding tussen metalen mogelijk?  Welk anion is normaal gesproken aanwezig in gedeïoniseerd water en kan worden neergeslagen door zilverionen?
Welk anion is normaal gesproken aanwezig in gedeïoniseerd water en kan worden neergeslagen door zilverionen?
 Dataproject beoordeelt hoe goed landen over de hele wereld de mensenrechten beschermen
Dataproject beoordeelt hoe goed landen over de hele wereld de mensenrechten beschermen  EU gaat twee van haar drie klimaatdoelen voor 2020 halen
EU gaat twee van haar drie klimaatdoelen voor 2020 halen Een diepzee-ecosysteem voeden:verrassend productieve microben zijn een belangrijke voedselbron in de afgrond
Een diepzee-ecosysteem voeden:verrassend productieve microben zijn een belangrijke voedselbron in de afgrond Plotselinge opwarming boven Antarctica om de droogte in Australië te verlengen
Plotselinge opwarming boven Antarctica om de droogte in Australië te verlengen Klimaatverandering beïnvloedt de manier waarop Europa overstroomt, experts waarschuwen
Klimaatverandering beïnvloedt de manier waarop Europa overstroomt, experts waarschuwen
Hoofdlijnen
- Red Delicious of Wolf-appel? Braziliaanse savannevruchten met een hoog gehalte aan antioxidanten
- Nestgebieden van schildpadden volgen
- Hoeveel verschillende peptiden kunnen worden gevormd door alle aminozuren slechts één keer te gebruiken?
- DNA-sterke binding:een langdurige verbintenis of veel korte relaties?
- Voedden primitieve walvisachtigen zich als zeereptielen?
- Wat zijn de functies van verschillende witte bloedcellen?
- Nieuwe bananenziekte verspreidt zich en vormt een bedreiging voor de voedselzekerheid van Afrika
- Hoe zangvogels een nieuw lied leren
- Waarom blozen mensen?
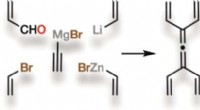
- Gespannen, symmetrisch, en nieuw:tetravinylalleen, een klein maar krachtig molecuul, is voor het eerst gesynthetiseerd
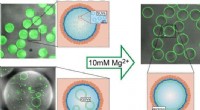
- Celachtige lipideblaasjes die kunnen worden gevuld met natuurlijke celeiwitten
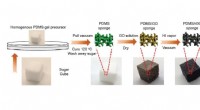
- Rekbare natrium-ion batterij-elektroden gemaakt van suikerklontjes
- Technische defecten in kristallijn materiaal verhogen de elektrische prestaties

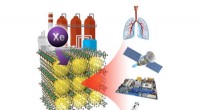
- Xenongas uit afvalstromen halen
 Kun je winterweer voorspellen op basis van zomerweer?
Kun je winterweer voorspellen op basis van zomerweer?  Ocean Plants in the Sunlight Zone
Ocean Plants in the Sunlight Zone  Antarctica:terugkeer van de Weddell-polynya ondersteunt het klimaatmodel van Kiel
Antarctica:terugkeer van de Weddell-polynya ondersteunt het klimaatmodel van Kiel Nieuw tijdperk voor New Norcia deep space-antenne
Nieuw tijdperk voor New Norcia deep space-antenne Onderzoekers houden onderzoek naar de houding ten opzichte van stadsdieren en waar mensen willen dat ze leven
Onderzoekers houden onderzoek naar de houding ten opzichte van stadsdieren en waar mensen willen dat ze leven  Hoe vrouwelijke hyena's de mannetjes gingen domineren
Hoe vrouwelijke hyena's de mannetjes gingen domineren  Hoe nummers te schrijven in standaardformulier
Hoe nummers te schrijven in standaardformulier  Welk type binding vormen glycineglucose en stearinezuur?
Welk type binding vormen glycineglucose en stearinezuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

