
Wetenschap
Als je naar het etiket op een fles zuur kijkt, hoe kun je dan zien of het geconcentreerd is of niet?
1. Concentratiepercentage :Het concentratiepercentage van een zuur staat meestal op het etiket aangegeven. Dit getal vertegenwoordigt de hoeveelheid zuur die in de oplossing aanwezig is, uitgedrukt als gewichts- of volumepercentage. Een 10% zoutzuuroplossing bevat bijvoorbeeld 10 gram zoutzuur in 100 gram oplossing. Hoe hoger het concentratiepercentage, hoe geconcentreerder het zuur.
2. Molariteit :De molariteit van een zuur is een andere maatstaf voor de concentratie ervan. Het vertegenwoordigt het aantal mol zuur dat aanwezig is in één liter oplossing. Een 1 molaire zoutzuuroplossing bevat bijvoorbeeld één mol zoutzuur in één liter oplossing. Hoe hoger de molariteit, hoe geconcentreerder het zuur.
3. pH-waarde :De pH-waarde van een zuur is een maatstaf voor de zuurgraad of basiciteit ervan. Het wordt uitgedrukt op een schaal van 0 tot 14, waarbij 0 het meest zuur is, 7 neutraal en 14 het meest basisch. Hoe lager de pH-waarde, hoe zuurder de oplossing. Geconcentreerde zuren hebben doorgaans een lagere pH-waarde dan verdunde zuren.
4. Uiterlijk :Geconcentreerde zuren zijn vaak stroperiger en hebben een sterkere geur dan verdunde zuren. Geconcentreerd zwavelzuur is bijvoorbeeld een dikke, olieachtige vloeistof met een sterke, scherpe geur, terwijl verdund zwavelzuur een heldere, waterige vloeistof is met een mildere geur.
5. Corrosiviteit :Geconcentreerde zuren zijn corrosiever dan verdunde zuren. Dit betekent dat ze meer schade kunnen veroorzaken aan materialen, zoals huid, metaal en kleding. Het is belangrijk om voorzichtig om te gaan met geconcentreerde zuren en geschikte beschermende kleding te dragen, zoals handschoenen en een veiligheidsbril.
 De volgende fase:neurale netwerken gebruiken om gasfasemoleculen te identificeren
De volgende fase:neurale netwerken gebruiken om gasfasemoleculen te identificeren Wat zijn de laboratoriumbereidingen van zuurstof met behulp van manganijdi-oxide?
Wat zijn de laboratoriumbereidingen van zuurstof met behulp van manganijdi-oxide?  Wetenschappers vinden een manier om langlevende, snelladende batterijen
Wetenschappers vinden een manier om langlevende, snelladende batterijen Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?
Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?  Koolstofbrandstoffen worden groen voor hernieuwbare energie
Koolstofbrandstoffen worden groen voor hernieuwbare energie
 NASA-NOAA's Suomi NPP-satelliet vangt tyfoon Yutu-versterking, Guam op scherp
NASA-NOAA's Suomi NPP-satelliet vangt tyfoon Yutu-versterking, Guam op scherp Hoe een vogel te maken voor een wetenschapsproject
Hoe een vogel te maken voor een wetenschapsproject  Een gematigd bioom en een taiga bioom vergelijken en contrasteren
Een gematigd bioom en een taiga bioom vergelijken en contrasteren  Darwin of Kimura? Natuurlijke selectie puur toeval? Nieuw literatuuronderzoek heeft tot doel een verhit debat te verhelderen
Darwin of Kimura? Natuurlijke selectie puur toeval? Nieuw literatuuronderzoek heeft tot doel een verhit debat te verhelderen  17% van de voedselproductie wereldwijd wordt verspild, VN-rapport schattingen
17% van de voedselproductie wereldwijd wordt verspild, VN-rapport schattingen
Hoofdlijnen
- Hoe planten 'slechte' moleculen benutten voor goede doeleinden
- Planning op meerdere schaalniveaus voor gezonde koralen en gemeenschappen
- Waarom vermijden de meeste wetenschappers wetenschappelijke theorieën wetten te noemen?
- Het SlTHM27-SlGAD2-model reguleert de koudetolerantie bij tomaat door GABA en anthocyanine te reguleren
- Kunnen uitwerpselen de soort redden?
- Nieuwe studie biedt mechanistische inzichten in hoe gentranscriptie wordt gereguleerd in zoogdiercellen
- Hoe zijn genen, DNA en chromosomen met elkaar verbonden?
- SARS-CoV-2:Hoe de geschiedenis van menselijke populaties hun immuunrespons beïnvloedt
- Welke hormoonachtige moleculen worden NIET uit arachidonzuur geproduceerd?
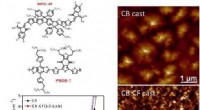
- Binair oplosmiddelmengsel dat het hoge rendement van polymere zonnecellen verhoogt
- Het maken van mazen met behulp van het Turings wiskundig model resulteert in efficiënte waterfilters

- Technologie verhoogt de output van microfluïdische onderzoeksgegevens 100-voudig

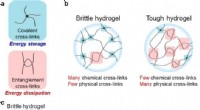
- Een universele methode om eenvoudig stevige en rekbare hydrogels te ontwerpen
- Verrode fluorescerende zijde kan schadelijke bacteriën doden als biomedische en milieuremedie
 Hoe calciumchloride en water te mengen
Hoe calciumchloride en water te mengen Forensische archeologen beginnen vermiste Spaanse Burgeroorlog terug te vinden
Forensische archeologen beginnen vermiste Spaanse Burgeroorlog terug te vinden Waarom mensen schreeuwen,
Waarom mensen schreeuwen,  Geluid
Geluid  Herstructurering van SAP van miljard euro naar kosten 4, 400 banen
Herstructurering van SAP van miljard euro naar kosten 4, 400 banen Astronaut Luca voelt de kracht, om rover controle te bevorderen
Astronaut Luca voelt de kracht, om rover controle te bevorderen Op licht gebaseerde productie van moleculen voor het ontdekken van geneesmiddelen
Op licht gebaseerde productie van moleculen voor het ontdekken van geneesmiddelen Natuurkundigen werpen nieuw licht op een oud kwantumopticaprobleem over collectief gedrag
Natuurkundigen werpen nieuw licht op een oud kwantumopticaprobleem over collectief gedrag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

