
Wetenschap
Wat is de massa van 5,23x1021 platina-atomen?
Om de massa van 5,23x1021 platina-atomen te berekenen, kunnen we de molaire massa van platina gebruiken. De molaire massa van platina is 195,084 g/mol, wat betekent dat één mol platina-atomen een massa heeft van 195,084 gram.
Eerst moeten we het aantal mol platina in 5,23x1021 atomen vinden. We kunnen dit doen door het aantal atomen te delen door het getal van Avogadro, dat is 6,022x1023 atomen/mol:
$$moles \ of \ Pt =\frac{5,23\times10^{21} \ atoms}{6,022\times10^{23} \ atomen/mol} =8,68\times10^{-3} \ mol$$
Nu kunnen we de molaire massa van platina gebruiken om de massa van 5,23x1021 platina-atomen te berekenen door het aantal mol te vermenigvuldigen met de molaire massa:
$$massa \ van \ Pt =8,68\times10^{-3} \ mol \times 195,084 \ g/mol =1,70 \ g$$
Daarom is de massa van 5,23x1021 platina-atomen 1,70 gram.
 Onderzoek toont aan hoe elektriciteitsetende microben elektronen gebruiken om koolstofdioxide te fixeren
Onderzoek toont aan hoe elektriciteitsetende microben elektronen gebruiken om koolstofdioxide te fixeren Ontwerp van kunstmatige cellen krijgt een boost met de lancering van FABRICELL
Ontwerp van kunstmatige cellen krijgt een boost met de lancering van FABRICELL Wetenschappers ontrafelen nieuwe inzichten in veelbelovend halfgeleidermateriaal
Wetenschappers ontrafelen nieuwe inzichten in veelbelovend halfgeleidermateriaal Radicale chemie maakt eenvoudige synthese van ethers mogelijk
Radicale chemie maakt eenvoudige synthese van ethers mogelijk Een aardappellamp maken
Een aardappellamp maken
 NASA-satelliet vindt 16W nu subtropisch
NASA-satelliet vindt 16W nu subtropisch Nieuwe ontdekkingen van diepzeedieren rechtvaardigen uitgebreide bescherming in Costa Ricaanse wateren
Nieuwe ontdekkingen van diepzeedieren rechtvaardigen uitgebreide bescherming in Costa Ricaanse wateren Zware sneeuwval veroorzaakt reischaos in Noord-Europa
Zware sneeuwval veroorzaakt reischaos in Noord-Europa Vaarwel ‘uitsterven’, hallo ‘vergankelijkheid’? Validatie van een nieuw paradigma
Vaarwel ‘uitsterven’, hallo ‘vergankelijkheid’? Validatie van een nieuw paradigma  Hoe passen woestijnplanten zich aan hun omgeving aan?
Hoe passen woestijnplanten zich aan hun omgeving aan?
Hoofdlijnen
- Stamcelvaccins: de nieuwe grens in kankertherapie?
- Huilende olifanten en giechelende ratten - dieren hebben gevoelens, te
- Hoe de squashlandbouw bijen verspreidde in het precolumbiaanse Noord-Amerika
- Nieuw wiskundig model:hoe gevaarlijke bacteriën kolonies vormen
- Delen mensen en bananen werkelijk 50 procent van hetzelfde DNA?
- Vraag en antwoord:De dood van Noordse walvissen leidt tot gesprekken over ecologie en maritieme veiligheid
- Onderzoeker onderzoekt waarom nakomelingen van oudere ouders de levensduur hebben verkort
- Hoe groter een kern is, hoe groter de kern is?
- Onderzoekers tonen aan dat sprinkhanen kanker bij de mens kunnen 'opsnuiven'
- Ontwikkeling van een enzym tegen antibioticaresistente miltvuur
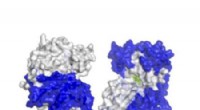
- Doorbraak in het benutten van de kracht van biologische katalysatoren

- Kleine oplichtende streepjescodes identificeren moleculen door hun fonkeling

- Overgebleven graan van brouwerijen kan worden omgezet in brandstof voor huizen

- Elektrische schok tot koolstof maakt een betere waterzuiveraar
 Wat is 250 Fahrenheit omgezet in Celsius?
Wat is 250 Fahrenheit omgezet in Celsius?  Hoe de aarde te verdedigen tegen asteroïden
Hoe de aarde te verdedigen tegen asteroïden  Wat betekent ijzerhoudende grond?
Wat betekent ijzerhoudende grond?  Wat zijn de vier belangrijkste soorten winden?
Wat zijn de vier belangrijkste soorten winden?  Hoe de pandemie van het coronavirus de perfecte storm van Florida werd
Hoe de pandemie van het coronavirus de perfecte storm van Florida werd Waarom invasieve mieren een stille bedreiging vormen voor onze ecosystemen
Waarom invasieve mieren een stille bedreiging vormen voor onze ecosystemen  Wat zijn de vier ecosysteemtypen?
Wat zijn de vier ecosysteemtypen?  Hoe China's deal met de VS hielp voorkomen dat klimaattoppen instortten
Hoe China's deal met de VS hielp voorkomen dat klimaattoppen instortten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

