
Wetenschap
Wat bedoel je als je zegt dat een atoom een tekort aan elektronen heeft?
Verbindingen met een tekort aan elektronen worden vaak aangetroffen in de coördinatiechemie, waar ze fungeren als Lewis-zuren door elektronenparen van andere moleculen of ionen te accepteren. Dit kan leiden tot de vorming van stabiele complexen, die belangrijk zijn bij veel biologische processen zoals zuurstoftransport en katalyse.
Enkele voorbeelden van elektronendeficiënte verbindingen zijn onder meer:
* Boortrifluoride (BF3)
* Koolmonoxide (CO)
* Stikstofmonoxide (NO)
* Zwaveldioxide (SO2)
Deze verbindingen zijn allemaal in staat elektronenparen van andere moleculen of ionen te accepteren en stabiele complexen te vormen. BF3 kan bijvoorbeeld reageren met ammoniak (NH3) om het complex BF3NH3 te vormen.
Verbindingen met een tekort aan elektronen zijn ook te vinden in de organische chemie, waar ze vaak carbokationen worden genoemd. Carbokationen zijn positief geladen koolstofatomen die een elektron missen. Ze zijn zeer reactief en kunnen een verscheidenheid aan reacties ondergaan, waaronder additie, substitutie en eliminatie.
Enkele voorbeelden van carbokaties zijn onder meer:
* Het methylkation (CH3+)
* Het ethylkation (C2H5+)
* Het tert-butylkation (C(CH3)3+)
Deze carbokationen zijn allemaal zeer reactief en kunnen verschillende reacties ondergaan. Het methylkation kan bijvoorbeeld reageren met water om methanol (CH3OH) te vormen.
Elektronendeficiënte verbindingen zijn belangrijk in een verscheidenheid aan chemische processen, en ze spelen een cruciale rol in veel biologische systemen.
 Chemische reacties doorbreken energiebarrières met behulp van flyby-trajecten
Chemische reacties doorbreken energiebarrières met behulp van flyby-trajecten Welke chemische stof komt vrij als bruispoeder wordt gemengd met water?
Welke chemische stof komt vrij als bruispoeder wordt gemengd met water?  Hoe de mondiale stromen van giftig kwik de menselijke gezondheid beïnvloeden
Hoe de mondiale stromen van giftig kwik de menselijke gezondheid beïnvloeden  Vormen twee koolstofatomen een niet-polaire covalente binding?
Vormen twee koolstofatomen een niet-polaire covalente binding?  Onderzoekers ontdekken efficiënte en duurzame manier om zout en metaalionen uit water te filteren
Onderzoekers ontdekken efficiënte en duurzame manier om zout en metaalionen uit water te filteren
 De werelden van ontoegankelijkheid zijn, nou ja, behoorlijk ontoegankelijk
De werelden van ontoegankelijkheid zijn, nou ja, behoorlijk ontoegankelijk Industriële microben kunnen vee voeden, varkens en kippen met minder schade aan het milieu
Industriële microben kunnen vee voeden, varkens en kippen met minder schade aan het milieu Extreme blootstelling aan hitte verergert ondervoeding bij kinderen
Extreme blootstelling aan hitte verergert ondervoeding bij kinderen Pesticiden en industriële verontreinigende stoffen gevonden in sneeuw bovenop Arctische gletsjers
Pesticiden en industriële verontreinigende stoffen gevonden in sneeuw bovenop Arctische gletsjers Moerassen zijn unieke records van de geschiedenis - hier is waarom
Moerassen zijn unieke records van de geschiedenis - hier is waarom
Hoofdlijnen
- Evolutionair celbiologisch onderzoek laat zien hoe de energieproductie kan worden geoptimaliseerd om snelle groei zonder ademhaling te garanderen
- Factoren die de groei van micro-organismen beïnvloeden
- Is hennep hetzelfde als marihuana?
- Welke Cell Organelle slaat DNA op en synthetiseert RNA?
- Eiwitsynthese in eukaryoten en prokaryoten?
- Uit onderzoek blijkt dat klimaatverandering tropische vissen helpt het Australische oceaanwater binnen te dringen
- Wat is het eindproduct van fotosynthese?
- Radiometrische datering: definitie, hoe werkt het, gebruik & voorbeelden
- Welke functies delen mitochondria en bacteriën?
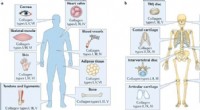
- Onderzoekers kwantificeren, karakteriseren en identificeren functies van collageen, zijn subtypes
- Kristallisatie opgehelderd, onderzoekers rapporteren

- Onderzoekers creëren kunstkraakbeen dat zichzelf kan herstellen

- Video:Vampierenfolklore heeft meer chemie dan je zou denken

- Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
 Mongolen drinken zuurstofcocktails tegen smog
Mongolen drinken zuurstofcocktails tegen smog Hoe kun je in een chemisch laboratorium benzoëzuur scheiden van para-nitro-aniline tijdens de extractie?
Hoe kun je in een chemisch laboratorium benzoëzuur scheiden van para-nitro-aniline tijdens de extractie?  Burgerwetenschappers ontdekken tientallen bruine dwergen
Burgerwetenschappers ontdekken tientallen bruine dwergen Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden
Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden Thuiswerken:hoe classisme het gesprek heimelijk domineerde
Thuiswerken:hoe classisme het gesprek heimelijk domineerde Ruimtestationproject probeert de middelen te kristalliseren om zenuwgif tegen te gaan
Ruimtestationproject probeert de middelen te kristalliseren om zenuwgif tegen te gaan Hoeveel atomen zitten er in 1 mol chloor?
Hoeveel atomen zitten er in 1 mol chloor?  Hoe een antistatische mat te testen met een meter
Hoe een antistatische mat te testen met een meter
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

