
Wetenschap
Wat is de procentuele opbrengst aan koolstofdisulfide als bij de reactie 33,4 g zwaveldioxide 10,1 g disulfide produceert?
1. Bepaal de theoretische opbrengst aan koolstofdisulfide.
2. Vergelijk de werkelijke opbrengst (10,1 g) met de theoretische opbrengst en druk het resultaat uit als een percentage.
1. Theoretisch rendement:
De uitgebalanceerde chemische vergelijking voor de reactie tussen zwaveldioxide en methaan om koolstofdisulfide te produceren is:
```
CO2 + 2H2S ---> CS2 + 2H2O
```
Uit de vergelijking kunnen we zien dat 1 mol CO2 reageert met 2 mol H2S om 1 mol CS2 te produceren.
De molaire massa van CS2 is 76 g/mol.
Daarom kan de theoretische opbrengst van CS2 als volgt worden berekend:
```
Theoretisch rendement =33,4 g SO2 * (1 mol SO2 / 64 g SO2) * (1 mol CS2 / 1 mol SO2) * (76 g CS2 / 1 mol CS2)
=40,9 gram CS2
```
2. Percentage opbrengst:
Het opbrengstpercentage wordt berekend door de werkelijke opbrengst te delen door de theoretische opbrengst en het resultaat met 100 te vermenigvuldigen.
```
Percentage opbrengst =(werkelijke opbrengst / theoretische opbrengst) * 100
=(10,1 g CS2 / 40,9 g CS2) * 100
=24,7%
```
Daarom bedraagt de procentuele opbrengst aan koolstofdisulfide 24,7%.
 Zelf-uitgezonden oppervlaktegolfingen in dynamische breuk van silicium eenkristal
Zelf-uitgezonden oppervlaktegolfingen in dynamische breuk van silicium eenkristal Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem
Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem Hoe gebruik je het woord alkalisch in een zin?
Hoe gebruik je het woord alkalisch in een zin?  Wat zijn de eigenschappen van rubber?
Wat zijn de eigenschappen van rubber?  Wanneer sommige ionische verbindingen oplossen, dissociëren niet al hun bindingen. Wat voor soort geleidbaarheid zou je verwachten dat een dergelijke oplossing zou hebben?
Wanneer sommige ionische verbindingen oplossen, dissociëren niet al hun bindingen. Wat voor soort geleidbaarheid zou je verwachten dat een dergelijke oplossing zou hebben?
 Amerikanen mochten in 2018 stemmen over veel energiemaatregelen - en verwierpen ze meestal
Amerikanen mochten in 2018 stemmen over veel energiemaatregelen - en verwierpen ze meestal Helpt het natuurbehoud door een prijs op de natuur te zetten?
Helpt het natuurbehoud door een prijs op de natuur te zetten?  Het mysterie oplossen waarom de koolstofdioxide in de atmosfeer tijdens ijstijden lager was
Het mysterie oplossen waarom de koolstofdioxide in de atmosfeer tijdens ijstijden lager was NASA analyseert kortstondige cycloon in de Golf van Bengalen
NASA analyseert kortstondige cycloon in de Golf van Bengalen Nigerianen eisen luchtkwaliteitsgegevens vanwege angst voor vervuiling
Nigerianen eisen luchtkwaliteitsgegevens vanwege angst voor vervuiling
Hoofdlijnen
- Wat bepaalt welke eiwitten de cel maakt?
- Onderzoekers ontdekken hoe dieren hun puntige lichaamsdelen laten groeien
- Verborgen of uitgestorven? Genoomanalyse van een 120 jaar oud exemplaar van torpedorog bevestigt de status van de soort
- Wat is de afbraak van sucrase?
- Wat is osmoregulatie en waarom is het belangrijk in levende organismen?
- Is intelligentie een genetisch kenmerk?
- Leg uit hoe mutatievariatie-adaptatie met elkaar verband houdt?
- Hoe visvinnen evolueerden vlak voor de overgang naar land
- De eerste stappen van een cel:een model bouwen om uit te leggen hoe cellen groeien
- Stazakken van hernieuwbare grondstoffen en nanocellulose

- Opgelost zout kan weer in elkaar worden gezet op nanoschaal, volgens simulaties

- Whisky verifiëren met laserlicht

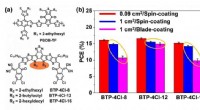
- Organische fotovoltaïsche cel met 17% efficiëntie en superieure verwerkbaarheid voor coatings op grote oppervlakken
- Onderzoekers ontwikkelen een manier om corrosie door ruwe olie beter te voorspellen

 Als je over een aardbeving vloog,
Als je over een aardbeving vloog,  5 landbouwtechnologieën die de wereld hebben veranderd
5 landbouwtechnologieën die de wereld hebben veranderd  NASA-infraroodbeeld toont Eugene nu een overblijfsel
NASA-infraroodbeeld toont Eugene nu een overblijfsel Wat is de prijs voor hydroniumion?
Wat is de prijs voor hydroniumion?  Hoe waarschijnlijk is het dat consumenten kunstmatige intelligentie zullen gebruiken voor bankadvies?
Hoe waarschijnlijk is het dat consumenten kunstmatige intelligentie zullen gebruiken voor bankadvies?  Taalkundigen voorspellen onbekende woorden met behulp van taalvergelijking
Taalkundigen voorspellen onbekende woorden met behulp van taalvergelijking Exoplaneten op ware grootte:nieuwe modelberekeningen tonen de impact van de helderheid van sterren en magnetische activiteit
Exoplaneten op ware grootte:nieuwe modelberekeningen tonen de impact van de helderheid van sterren en magnetische activiteit  Groene kerstdagen:Alpenskigebieden denken na over een toekomst zonder sneeuw
Groene kerstdagen:Alpenskigebieden denken na over een toekomst zonder sneeuw
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

