
Wetenschap
Als voor 1,25 gram zuiver CaCO3 25,5 ml HCl-oplossing nodig is voor een volledige reactie, wat is dan de molariteitsoplossing?
De uitgebalanceerde chemische vergelijking voor de reactie tussen CaCO3 en HCl is:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g)
Uit de vergelijking kunnen we zien dat 1 mol CaCO3 reageert met 2 mol HCl. De molaire massa van CaCO3 is 100,09 g/mol, dus 1,25 gram CaCO3 is gelijk aan 1,25 / 100,09 =0,0125 mol CaCO3.
Omdat 0,0125 mol CaCO3 reageert met 25,5 ml HCl-oplossing, kan de molariteit van de HCl-oplossing als volgt worden berekend:
Molariteit =mol opgeloste stof / volume oplossing in liters
Molariteit =0,0125 mol / (25,5 ml / 1000) L
Molariteit =0,0125 mol / 0,0255 L
Molariteit =0,489 M
Daarom is de molariteit van de HCl-oplossing 0,489 M.
 Hoe verschilt de zuurconcentratie van de sterkte van een zuur?
Hoe verschilt de zuurconcentratie van de sterkte van een zuur?  Hoe Luminol werkt
Hoe Luminol werkt  Zal het smeltpunt van ijs stijgen of dalen als er zout aan wordt toegevoegd?
Zal het smeltpunt van ijs stijgen of dalen als er zout aan wordt toegevoegd?  Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan
Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan Elektrisch geleidende verven en andere polymeerlegeringen nu gemakkelijk te produceren
Elektrisch geleidende verven en andere polymeerlegeringen nu gemakkelijk te produceren
 Van auto's tot Mars:wat goed is voor F1 is goed voor het leven in het hele universum
Van auto's tot Mars:wat goed is voor F1 is goed voor het leven in het hele universum Gaan er meer Australische bomen dood door droogte? Wetenschappers hebben jouw hulp nodig bij het spotten van dode bomen
Gaan er meer Australische bomen dood door droogte? Wetenschappers hebben jouw hulp nodig bij het spotten van dode bomen Bevroren in de tijd:oude schilderijen en nieuwe foto's laten zien dat sommige Nieuw-Zeelandse gletsjers binnenkort mogelijk zullen uitsterven
Bevroren in de tijd:oude schilderijen en nieuwe foto's laten zien dat sommige Nieuw-Zeelandse gletsjers binnenkort mogelijk zullen uitsterven  Nieuwe studie onthult het geheim van magmatische gesteenten die uit slechts één mineraal bestaan
Nieuwe studie onthult het geheim van magmatische gesteenten die uit slechts één mineraal bestaan Terug op het menu? Europeanen aten ooit zeewier, zo blijkt uit onderzoek
Terug op het menu? Europeanen aten ooit zeewier, zo blijkt uit onderzoek
Hoofdlijnen
- Enorme DNA-levensboom voor planten onthuld door een mondiaal wetenschappelijk team met behulp van 1,8 miljard letters genetische code
- Hoe heet het gedeeltelijk menselijke skelet dat onze hersenen beschermt?
- Wat veroorzaakt de dubbele helix om te draaien in een DNA-afbeelding?
- Continentale controles nodig om de strijd tegen boomziekten te handhaven
- Mariene microplastics:hoe de verspreiding van watermassa de transporttrajecten beïnvloedt
- Wat betekent de gedeeltelijke militaire mobilisatie van Rusland?
- Gezondheidsonderzoekers visualiseren een leven in silico
- De adder-nabootsende slang uit Azië is een unieke tak in de evolutionaire boom van reptielen
- Hoe wetenschappers infectieveroorzakende biofilms bestrijden
- Bruggen bouwen in de cel – met licht
- In het laboratorium gekweekt weefsel volgen met licht

- Pas op voor mede-bacteriën die geschenken dragen:onderzoek presenteert nieuwe potentiële antimicrobiële middelen
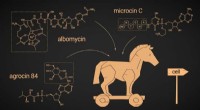
- Helicaten ontmoeten rotaxanen om belofte te creëren voor toekomstige ziektebehandeling

- Onderzoekers maken de eerste kaarten van twee melatoninereceptoren die essentieel zijn voor slaap
 Klik niet op die link! Hoe criminelen toegang krijgen tot uw digitale apparaten en wat er gebeurt als ze dat doen
Klik niet op die link! Hoe criminelen toegang krijgen tot uw digitale apparaten en wat er gebeurt als ze dat doen Wat is de energie van een foton 325nm?
Wat is de energie van een foton 325nm?  Onderzoek toont aan hoe klimaatverandering de gezondheid bedreigt
Onderzoek toont aan hoe klimaatverandering de gezondheid bedreigt  Mensen nemen irrationele beslissingen rationeel
Mensen nemen irrationele beslissingen rationeel Onderzoekers gebruiken schuifkrachten om zelf-geassembleerde supramoleculaire hydrogel te maken
Onderzoekers gebruiken schuifkrachten om zelf-geassembleerde supramoleculaire hydrogel te maken Waarom leven sommige microben in je darmen en andere niet?
Waarom leven sommige microben in je darmen en andere niet?  Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC)
Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC) Wetenschappelijke benadering van het testen van ideeën helpt startups te falen en sneller te schalen
Wetenschappelijke benadering van het testen van ideeën helpt startups te falen en sneller te schalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

