
Wetenschap
Hoe beïnvloedt een zuur de indicator?
De indicator fenolftaleïne is bijvoorbeeld kleurloos in zure oplossingen en roze in basische oplossingen. Dit komt omdat de door het zuur gedoneerde H+-ionen het fenolftaleïnemolecuul protoneren, waardoor de chemische structuur ervan verandert en ervoor zorgt dat het licht in het zichtbare spectrum absorbeert.
De kleurverandering van een indicator kan worden gebruikt om de pH van een oplossing te bepalen. Dit komt omdat elke indicator een specifiek pH-bereik heeft waarover hij van kleur verandert. Door de kleur van de indicator te vergelijken met een kleurenkaart, kunt u de pH van de oplossing bepalen.
Indicatoren zijn een belangrijk hulpmiddel in de chemie, omdat ze ons in staat stellen gemakkelijk en snel de pH van een oplossing te bepalen. Deze informatie kan worden gebruikt om de pH van een oplossing voor verschillende doeleinden te regelen, zoals in de voedingsindustrie, de farmaceutische industrie en de waterbehandelingsindustrie.
 Vervuiling van afvalwater:waarom de Britse waterindustrie kapot is
Vervuiling van afvalwater:waarom de Britse waterindustrie kapot is Populisme kan de democratie degraderen, maar is in opkomst – de oorzaken ervan en hoe deze worden verzwakt
Populisme kan de democratie degraderen, maar is in opkomst – de oorzaken ervan en hoe deze worden verzwakt  Nieuw onderzoek toont aan dat de Kīlauea-vulkaan in 2018 als een stompraket uitbarstte
Nieuw onderzoek toont aan dat de Kīlauea-vulkaan in 2018 als een stompraket uitbarstte  Kan deze vogel zich aanpassen aan een warmer klimaat? Lees de genen en ontdek het
Kan deze vogel zich aanpassen aan een warmer klimaat? Lees de genen en ontdek het  The Difference Between Tornadoes & Hurricanes
The Difference Between Tornadoes & Hurricanes
Hoofdlijnen
- Verbetering van statistische methoden om populaties wilde dieren te beschermen
- Het strandweer is hier en dat geldt ook voor haaien. Wetenschappers zeggen dat het tijd is om uit te kijken naar grote witte exemplaren
- Percepties van bewoners over de halsbandparkiet in Groot-Brittannië
- Wat zijn drie primaire doelen van mitose?
- Wat is de Western Blot-test?
- Hoe werd een eeuwenoude plant uit Latijns-Amerika het op een na belangrijkste marktgewas van Azië?
- Daling van huismus in verband met luchtvervuiling en slechte voeding
- Onderzoekers houden onderzoek naar de houding ten opzichte van stadsdieren en waar mensen willen dat ze leven
- Herenbaarden dragen meer bacteriën dan hondenbont,
- Legeronderzoek maakt de weg vrij voor nieuwe materialen

- Onderzoekers ontdekken een nieuwe route om complexe kristallen te vormen

- Een niet-destructieve methode voor het analyseren van oud-Egyptisch balsemmateriaal

- Nieuwe RNA-modificerende tool corrigeert genetische ziekten, inclusief aanjager van triple-negatieve borstkanker

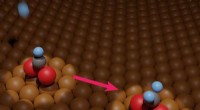
- Op heterdaad betrapt:belangrijke chemische tussenproducten bij de reactie van verontreinigende stof tot brandstof geïdentificeerd
 Hoe u een overspanningsbeveiliging kiest
Hoe u een overspanningsbeveiliging kiest  Drijvende parken gemaakt van plastic afval kunnen gemeenschappen verenigen om vervuiling aan te pakken
Drijvende parken gemaakt van plastic afval kunnen gemeenschappen verenigen om vervuiling aan te pakken De mysteries van supergeleiders onthullen:de nieuwe reikwijdte van Teams wordt nader bekeken
De mysteries van supergeleiders onthullen:de nieuwe reikwijdte van Teams wordt nader bekeken De Tarantulanevel zou geen sterren moeten vormen. Wat is er aan de hand?
De Tarantulanevel zou geen sterren moeten vormen. Wat is er aan de hand?  Socioloog legt uit hoe coronavirus de wereld om ons heen kan veranderen
Socioloog legt uit hoe coronavirus de wereld om ons heen kan veranderen Bananenplantenextract kan de sleutel zijn tot romiger, langer houdbaar ijs
Bananenplantenextract kan de sleutel zijn tot romiger, langer houdbaar ijs Regenbuien maken binnen enkele dagen een einde aan de bosbranden in Australië
Regenbuien maken binnen enkele dagen een einde aan de bosbranden in Australië Transformatorrobots op microschaal bundelen hun krachten om geblokkeerde slagaders te doorbreken
Transformatorrobots op microschaal bundelen hun krachten om geblokkeerde slagaders te doorbreken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

