
Wetenschap
Wat is de pH van een oplossing waarbij h plus gelijk is aan 7,0 x 10-2?
Om de pH van een oplossing te bepalen, gebruiken we de formule:
$$pH =-\log[H^+]$$
waarbij [H^+] de waterstofionenconcentratie in mol per liter (mol/L) voorstelt.
Gegeven [H^+] =7,0 x 10-2 mol/L, kunnen we de pH berekenen:
$$pH =-\log(7,0 \times 10^{-2}) \circa 1,15$$
Daarom is de pH van de oplossing ongeveer 1,15.
 Science Fair-onderwerpen met Glow Sticks
Science Fair-onderwerpen met Glow Sticks Wat is het verschil tussen zuren en antacida?
Wat is het verschil tussen zuren en antacida?  Synthese van waardevolle chemicaliën uit verontreinigde grond
Synthese van waardevolle chemicaliën uit verontreinigde grond Hoe zou je een stripverhaal maken waarin suiker verandert van vast naar vloeibaar?
Hoe zou je een stripverhaal maken waarin suiker verandert van vast naar vloeibaar?  Hardnekkige biofilms wegspoelen met reinigingsproducten voor schimmels
Hardnekkige biofilms wegspoelen met reinigingsproducten voor schimmels
Hoofdlijnen
- Wat is de fase in de mitose waarin het kernmembraan verdwijnt?
- DNA van bevroren dierentuin kan uitsterven van soorten voorkomen
- Waarom zijn chromosomen belangrijk voor celdeling?
- Uit een 20-jarig onderzoek blijkt hoe een gevestigd bedrijf, dat overschakelde van een product- naar een ecosysteemstrategie, zijn markt domineerde
- Hoe houdt de pH verband met de proliferatie van micro-organismen?
- Herpesvirussen en tumoren zijn geëvolueerd om te leren hoe hetzelfde oude RNA kan worden gemanipuleerd
- Hoe verhoudt het scheppingsverhaal zich tot de celtheorie?
- Octopussen gestrand op het strand van Wales - hier zijn de wetenschappelijke theorieën waarom
- Noemen olifanten 'mensen!'?
- filmpje:natto, de stinkende, slijmerige sojabonensnack

- Röntgenbeeldvorming onthult inzichten in een natuurlijke mug-dodende verbinding

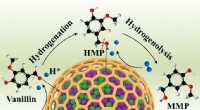
- Ingekapselde nanodeeltjes van NiCo-legeringen die HDO-reacties katalyseren
- Stal, zelfverstorende microbellen als intraveneuze zuurstofdragers

- Video:Wat is het noorderlicht?

 Hoe de vernietiging van het oude Palmyra door de Islamitische Staten zich afspeelde op Arabisch Twitter
Hoe de vernietiging van het oude Palmyra door de Islamitische Staten zich afspeelde op Arabisch Twitter Virgin Galactics volgende ruimteschip bereikt mijlpaal in bouw
Virgin Galactics volgende ruimteschip bereikt mijlpaal in bouw Eigenaren van waterputten moeten goed testen na een overstroming
Eigenaren van waterputten moeten goed testen na een overstroming de reactie tussen cokes en zout?
de reactie tussen cokes en zout?  Miljoenen microdeeltjes in een oogwenk microprinten via multi-foton 3D-laserprinten
Miljoenen microdeeltjes in een oogwenk microprinten via multi-foton 3D-laserprinten  Wat zijn stablecoins? Een blockchain-expert legt uit
Wat zijn stablecoins? Een blockchain-expert legt uit Onderzoeker onderzoekt hoe mensen onderbrekingen in een gesprek ervaren
Onderzoeker onderzoekt hoe mensen onderbrekingen in een gesprek ervaren Waarom is water belangrijk voor het leven?
Waarom is water belangrijk voor het leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

