
Wetenschap
Wat is het oxidatiegetal voor H3PO2?
- Waterstof (H) heeft in de meeste verbindingen doorgaans een oxidatiegetal van +1, behalve in metaalhydriden waar dit -1 kan zijn. In dit geval geven we er +1 aan.
- Zuurstof (O) heeft in verbindingen doorgaans een oxidatiegetal van -2.
- Fosfor (P) is het centrale atoom, dus het oxidatiegetal is variabel en moet worden bepaald.
Met behulp van de volgende formule kunnen we het oxidatiegetal van P berekenen:
\(Lading\ van\ het\ molecuul =\som (Oxidatie\aantallen\ van\individuele\ atomen\maal hun\ respectieve\tellingen) \)
De lading van H3PO2 is 0 omdat het een neutraal molecuul is.
De toegewezen oxidatienummers invoeren:
\( 0 =(3 \maal +1) + (2 \maal -2) + (1 \maal Oxidatie\ aantal\ van\ P) \)
Vereenvoudiging van de vergelijking:
\( 0 =+3 -4 + Oxidatie\ aantal\ van\ P \)
\( Oxidatie\ aantal\ van\ P =+4 -3 =+1\)
Daarom is het oxidatiegetal van fosfor in H3PO2 +1.
 Experimenten met rauw ei en azijn
Experimenten met rauw ei en azijn  Groene chemici vinden een manier om cashewnootdoppen om te zetten in zonnebrandcrème
Groene chemici vinden een manier om cashewnootdoppen om te zetten in zonnebrandcrème Onderzoekers maken de eerste rietjes met polyhydroxyalkanoaat (PHA) plastic
Onderzoekers maken de eerste rietjes met polyhydroxyalkanoaat (PHA) plastic Wat is de relatie tussen temperatuur en oplosbaarheid voor kno3?
Wat is de relatie tussen temperatuur en oplosbaarheid voor kno3?  Snelle ontwerpmethode voor mini-eiwitten opent de weg om een nieuwe klasse geneesmiddelen te creëren
Snelle ontwerpmethode voor mini-eiwitten opent de weg om een nieuwe klasse geneesmiddelen te creëren
 New York zou plastic schuimcontainers over de hele staat kunnen verbieden onder het voorstel van Cuomo
New York zou plastic schuimcontainers over de hele staat kunnen verbieden onder het voorstel van Cuomo Hiaten in de gegevens belemmeren de monitoring van zware metalen die Arctische gemeenschappen bedreigen
Hiaten in de gegevens belemmeren de monitoring van zware metalen die Arctische gemeenschappen bedreigen Koude fronteffecten op de windrichting
Koude fronteffecten op de windrichting  Californië onderneemt actie om meer plastic afval te verminderen, waaronder zakken voor boodschappen
Californië onderneemt actie om meer plastic afval te verminderen, waaronder zakken voor boodschappen Irma veroorzaakt ongebruikelijke stormvloeden aan beide kusten van Florida
Irma veroorzaakt ongebruikelijke stormvloeden aan beide kusten van Florida
Hoofdlijnen
- Behouden zowel dierlijke als plantaardige cellen het vermogen om zich gedurende hun hele leven te differentiëren?
- Vier nieuwe caladiumcultivars voor containers en landschappen
- Hoe onderhoudt een cel homeostase?
- Waar bevinden zich de 6 biomen?
- Mannelijke spinnen laten zich van hun gevoelige kant zien
- Het lichaam over zeer efficiënte interne afweermechanismen beschikt die elke hoeveelheid ongewenste stoffen kunnen verwijderen?
- Hoe zal de aarde er over 50 uitzien,
- Onderzoeksteam ontwikkelt versneld proces voor genetische verbetering van planteigenschappen
- 3 fasen van interfase
- Ammoniaksynthese - de grootste innovatie van de 20e eeuw

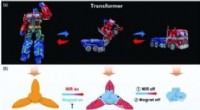
- Magnetisch gestuurd, op hydrogel gebaseerde slimme transformatoren
- Afstembare omgekeerde fotochromen in vaste toestand

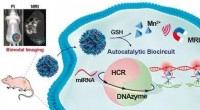
- Amplificatie en beeldvorming van microRNA als biomarker om tumorontwikkeling te detecteren
- Hout gebruiken in elektroden voor duurzamer, duurzame wearables

 Gebruik van Calculus in het dagelijks leven
Gebruik van Calculus in het dagelijks leven Wat zijn trends tussen de elementen voor atomaire grootte?
Wat zijn trends tussen de elementen voor atomaire grootte?  Horizontaal hardlopen kan maanastronauten helpen hun fysieke conditie te behouden
Horizontaal hardlopen kan maanastronauten helpen hun fysieke conditie te behouden  Metalen array om de volgende generatie true-3D-near-eye-displays mogelijk te maken
Metalen array om de volgende generatie true-3D-near-eye-displays mogelijk te maken  Asteroïde orus occultatie voor het eerst waargenomen door eVscope
Asteroïde orus occultatie voor het eerst waargenomen door eVscope Hebben geslacht, etniciteit en opleiding invloed op het vermogen van mensen om een baan te krijgen die bij hun interesses past?
Hebben geslacht, etniciteit en opleiding invloed op het vermogen van mensen om een baan te krijgen die bij hun interesses past?  Hoe bedrijven werknemers het beste kunnen helpen de verbinding met hun werk te verbreken
Hoe bedrijven werknemers het beste kunnen helpen de verbinding met hun werk te verbreken Op sociale media, pleeggezinnen deelden hun zorgen over pandemie
Op sociale media, pleeggezinnen deelden hun zorgen over pandemie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

