
Wetenschap
Is de pH afhankelijk van de concentratie van de verbinding?
Temperatuur kan ook de pH van een oplossing beïnvloeden. Over het algemeen neemt de pH van een oplossing af bij toenemende temperatuur. Dit komt omdat de dissociatiesnelheid van watermoleculen toeneemt bij toenemende temperatuur, wat leidt tot een hogere concentratie waterstofionen in de oplossing.
De concentratie van andere verbindingen in de oplossing kan ook de pH beïnvloeden. De aanwezigheid van sterke zuren of basen kan bijvoorbeeld de pH van de oplossing aanzienlijk veranderen.
Voor een bepaalde verbinding is er een specifieke concentratie waarbij de pH van de oplossing een merkbare verandering vertoont. In de context van zwakke zuren en basen komt deze specifieke concentratie gewoonlijk overeen met respectievelijk de pKa- of pKb-waarde van de verbinding.
 Nieuwe techniek maakt het gemakkelijker om te bepalen hoe menselijke voorouders vuur gebruikten
Nieuwe techniek maakt het gemakkelijker om te bepalen hoe menselijke voorouders vuur gebruikten  Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel?
Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel? Onderzoekers ontdekken aanvullend bewijs voor enorme zonnestormen
Onderzoekers ontdekken aanvullend bewijs voor enorme zonnestormen Nieuwe lessen uit de ergste olieramp ooit
Nieuwe lessen uit de ergste olieramp ooit Wat zijn de vier ecosysteemtypen?
Wat zijn de vier ecosysteemtypen?
Hoofdlijnen
- Is er een gen voor elke ziekte?
- Wetenschappers ontdekken wat een gepantserde dinosaurus at tijdens zijn laatste maaltijd
- Ontsnapte GGO-canolaplanten blijven langdurig bestaan, maar verliezen mogelijk hun technische resistentie tegen pesticiden
- Hoe hotspots van genetische variatie zich ontwikkelden in menselijk DNA
- Hoe transporteren dragereiwitten stoffen door het celmembraan?
- Nest van bedreigde reuzenweekschildpad gevonden in Cambodja
- Een geneesmiddel tegen de ineenstorting van de honingbijkolonie?
- Haaienvinnenverboden helpen haaien misschien niet, wetenschappers zeggen:
- Waar in de cel vindt transcriptie en vertaling plaats?
- Een thermisch isolerend composiet van holle silicadeeltjes gemengd met cellulosevezels

- draaien, flexibele kristallen sleutel tot zonne-energieproductie

- Dominerende schimmel zou een oplossing kunnen zijn om meer biobrandstoffen en chemicaliën te produceren
- Eenvoudig proces haalt waardevol magnesiumzout uit zeewater

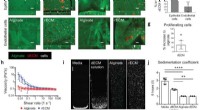
- Nieuwe bioink brengt 3D-printen van menselijke organen dichter bij de realiteit
 Verschillen tussen lichaamscellen en neuronen
Verschillen tussen lichaamscellen en neuronen Hoe vogels met verschillende veren samenkomen
Hoe vogels met verschillende veren samenkomen  Peru onthult gigantische kattenets op beroemde Nazca-site
Peru onthult gigantische kattenets op beroemde Nazca-site NASA ziet tropische depressie Jongdari uitgerekt
NASA ziet tropische depressie Jongdari uitgerekt Stortbuien van stortregens komen vaker voor met opwarming van de aarde
Stortbuien van stortregens komen vaker voor met opwarming van de aarde Geluidsoverlast het hardst in zwarte wijken, gescheiden steden
Geluidsoverlast het hardst in zwarte wijken, gescheiden steden Ontdekking vergroot het begrip van hoe sommige virussen zich vermenigvuldigen
Ontdekking vergroot het begrip van hoe sommige virussen zich vermenigvuldigen  Hoe vermijden ruimtetelescopen orbitaal puin?
Hoe vermijden ruimtetelescopen orbitaal puin?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

