
Wetenschap
Wat is de procentuele samenstelling van calciumfluoride?
Percentage samenstelling =(massa van element/totale massa) x 100
Aangezien calciumfluoride bestaat uit calcium (Ca) en fluor (F), moeten we hun atoommassa’s kennen:
Atoommassa van Ca =40,078 g/mol
Atoommassa van F =18,998 g/mol
In calciumfluoride zijn er één calciumatoom en twee fluoratomen. We moeten dus de molaire massa van calciumfluoride berekenen:
Molaire massa =(1 x atoommassa van Ca) + (2 x atoommassa van F)
=(1 x 40,078 g/mol) + (2 x 18,998 g/mol)
=78,074 g/mol
Nu kunnen we de procentuele samenstelling van calcium en fluor in calciumfluoride berekenen:
Percentage calcium =(massa calcium/molaire massa) x 100
=(40,078 g/mol / 78,074 g/mol) x 100
=51,35%
Percentage fluor =(massa fluor/molaire massa) x 100
=(2 x 18,998 g/mol / 78,074 g/mol) x 100
=48,65%
Daarom is de procentuele samenstelling van calciumfluoride 51,35% calcium en 48,65% fluor.
 Wat voor soort reactie is de vorming van ATP uit ADP?
Wat voor soort reactie is de vorming van ATP uit ADP?  Van identificatie tot chemische vingerafdruk voor explosieven in forensisch onderzoek
Van identificatie tot chemische vingerafdruk voor explosieven in forensisch onderzoek Polyethyleenproductieproces met hoge dichtheid
Polyethyleenproductieproces met hoge dichtheid Onverwacht nieuw materiaal is afgeschrikt tot omgevingsdruk
Onverwacht nieuw materiaal is afgeschrikt tot omgevingsdruk Wetenschappers brengen polymeren in focus op atomaire schaal
Wetenschappers brengen polymeren in focus op atomaire schaal
 Word weer mens om sociale, milieu-uitdagingen
Word weer mens om sociale, milieu-uitdagingen Californië wildvuur ontploft, brandend over 25 mijl in dag
Californië wildvuur ontploft, brandend over 25 mijl in dag Door de onverwachte landbouwproductie kon de pre-Spaanse samenleving floreren in de dorre Andes
Door de onverwachte landbouwproductie kon de pre-Spaanse samenleving floreren in de dorre Andes Hoe zag de vroege aarde eruit? Bijna zoals Venus, uit onderzoek blijkt
Hoe zag de vroege aarde eruit? Bijna zoals Venus, uit onderzoek blijkt Waarom komt er rook uit een brand?
Waarom komt er rook uit een brand?
Hoofdlijnen
- Welk type mensen leven in het chaparral-bioom?
- Uit welk monomeer bestaat het enzym?
- 195 manieren om de geschilderde dames van Californië te helpen:nieuwe voedselbronnen bieden hoop voor bedreigde vlinders
- Nieuw ontdekt eiwit kan worden gebruikt om levensreddende antischimmelmiddelen te produceren
- De opkomst van microbiële valsspelers in ijzerarme omgevingen:onderzoek onthult hun evolutionaire geschiedenis
- Houdt uw hond van u?
- Houden mannelijke vissen ze liever groot en kleurrijk?
- De enzymstructuur onthult hoe DNA wordt opengesteld voor transcriptie
- Zijn weg naar de top vinden:hoe een celoppervlakreceptor zijn bestemming bereikt
- Chemici bereiken doorbraak in de productie van driedimensionale moleculaire structuren

- Loodhalogenide perovskieten met verbeterde luminescentie en stabiliteit
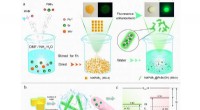
- Bio-geïnspireerd materiaal richt zich op uraniumvoorraden in oceanen voor duurzame kernenergie
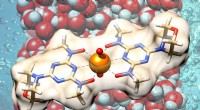
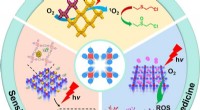
- Recente vorderingen in de ontwikkeling van foto- en elektroactieve waterstofgebonden organische raamwerken
- 'S Werelds beste gouden exemplaar onderzocht met Los Alamos-neutronen

 Wetenschappers laten zien dat er inderdaad sprake is van een ‘entropie’ van kwantumverstrengeling
Wetenschappers laten zien dat er inderdaad sprake is van een ‘entropie’ van kwantumverstrengeling  Elektrisch afstembare meta-oppervlakken effenen de weg naar dynamische hologrammen
Elektrisch afstembare meta-oppervlakken effenen de weg naar dynamische hologrammen Vulkaan barst uit in Indonesië, alarmniveau verhoogd naar hoogste niveau
Vulkaan barst uit in Indonesië, alarmniveau verhoogd naar hoogste niveau  James Webb Space Telescope om atmosferen van gasreuzen exoplaneten te inspecteren
James Webb Space Telescope om atmosferen van gasreuzen exoplaneten te inspecteren Hoe Newtons wiegen werken
Hoe Newtons wiegen werken  Welke factoren ondersteunen de evolutie?
Welke factoren ondersteunen de evolutie?  De merkwaardige geschiedenis van de opkomst en ondergang van twee aparte bedden
De merkwaardige geschiedenis van de opkomst en ondergang van twee aparte bedden Tot op de bodem uitzoeken:kan mijnbouw in de diepzee duurzaam zijn?
Tot op de bodem uitzoeken:kan mijnbouw in de diepzee duurzaam zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

