
Wetenschap
Naarmate de temperatuur van een gas met een vast volume toeneemt, zal de druk toenemen.
Naarmate de temperatuur van een gas met een vast volume toeneemt, zal de druk ook toenemen. Dit komt omdat naarmate de temperatuur van een gas stijgt, de moleculen sneller bewegen en vaker en met meer kracht tegen de wanden van de container botsen, waardoor een grotere druk op de container wordt uitgeoefend. De relatie tussen temperatuur en druk in een gas met een vast volume is direct proportioneel, wat betekent dat naarmate de temperatuur stijgt, de druk toeneemt, en omgekeerd. Deze relatie staat bekend als de wet van Boyle of de wet van Boyle-Mariotte.
 Een groot deel van de aarde is nog steeds wild, maar bedreigd door fragmentatie
Een groot deel van de aarde is nog steeds wild, maar bedreigd door fragmentatie Onwillige held? Schonere vissen laten zien dat het loont om onbaatzuchtig te zijn
Onwillige held? Schonere vissen laten zien dat het loont om onbaatzuchtig te zijn  Demonstranten Hawaï beloven langdurige strijd tegen telescoop
Demonstranten Hawaï beloven langdurige strijd tegen telescoop Arctische kwikniveaus dalen tijdens de diepten van de winter
Arctische kwikniveaus dalen tijdens de diepten van de winter Wat zijn de structurele aanpassingen van een vlinder?
Wat zijn de structurele aanpassingen van een vlinder?
Hoofdlijnen
- Waarom hebben we hondsdolheid nog niet uitgeroeid?
- In ons lichaam zijn teams van microben aan het werk. Onderzoekers hebben ontdekt waar ze mee bezig zijn.
- Geurdetectiehonden onderscheiden geurmoleculen beter dan eerder werd gedacht
- Natuur of opvoeding:hoe komt een dier aan zijn microbioom?
- Hommels kunnen volgens de Californische instandhoudingswet als vissen worden geclassificeerd, zegt de rechtbank
- 7 soorten bindweefsel
- Onderzoek toont aan hoe chimpansees vaardigheden delen
- Onderzoek lost de puzzel op waarom de hommel zo goed kan vliegen
- Er zwerven nog steeds ruim 2 miljoen gazellen over de Mongoolse steppe
- Enzymcocktail ontwikkeld in Brazilië stimuleert de productie van ethanol van de tweede generatie

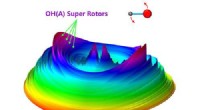
- Laser onthult elektronisch geëxciteerde hydroxyl-superrotors in waterfotochemie
- Video:Wat is een elektron?

- Duurzamere recycling van kunststoffen

- Mysterieuze micro-eiwitten hebben grote gevolgen voor menselijke ziekten
 Supramoleculaire complexvorming - antraceen macrocyclus en C60 fullereen
Supramoleculaire complexvorming - antraceen macrocyclus en C60 fullereen Onderzoekers gebruiken LiDAR om invasieve vissen te lokaliseren en een nationale schat te behouden
Onderzoekers gebruiken LiDAR om invasieve vissen te lokaliseren en een nationale schat te behouden Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen
Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen Op weg naar stabiele zelfmontage
Op weg naar stabiele zelfmontage Is CaSO4 ionisch of covalent gebonden?
Is CaSO4 ionisch of covalent gebonden?  NASA's Terra Satellite vindt krachtige stormen in orkaan Hector
NASA's Terra Satellite vindt krachtige stormen in orkaan Hector Archeoloog ontkracht de mythe van de bijna naakte Bosjesmannen
Archeoloog ontkracht de mythe van de bijna naakte Bosjesmannen Neutrino's leveren het eerste experimentele bewijs op van gekatalyseerde fusie die dominant is in veel sterren
Neutrino's leveren het eerste experimentele bewijs op van gekatalyseerde fusie die dominant is in veel sterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

