
Wetenschap
Kan NH3 functioneren als een bronsted-lowry-basis?
Ja, NH3 kan functioneren als Bronsted-Lowry-basis.
Een Bronsted-Lowry-base is een stof die een proton (H+) kan accepteren. NH3 kan een proton accepteren om NH4+ (ammoniumion) te vormen, dus het is een Bronsted-Lowry-base.
De reactie van NH3 met H+ om NH4+ te vormen kan als volgt worden weergegeven:
NH3 + H+ → NH4+
Bij deze reactie accepteert NH3 een proton uit H+ om NH4+ te vormen. Daarom is NH3 een Bronsted-Lowry-base.
Hoofdlijnen
- Squash-variëteit waarvan ooit werd gedacht dat ze uitgestorven was, gedijt goed op biologische boerderij
- Hoe het boren naar olie in het Arctic National Wildlife Refuge van invloed kan zijn op dieren in het wild
- Het verschil tussen glycolyse en gluconeogenese
- Hoe de ‘loopbandband’ zorgt voor een goede celdeling
- Dodelijke hersenziekte gevonden bij twee Californische herten
- Bioloog uit Syracuse onthult hoe walvissen kunnen 'zingen' voor hun avondeten
- Hoe planten vrienden worden met schimmels
- Amerikaanse biologische klok-genetici winnen Nobelprijs voor Geneeskunde 2017
- Wat zijn de vijanden van een Blauwe Morpho-vlinder?
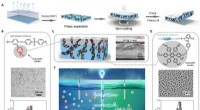
- Een efficiëntere op membraan gebaseerde generator voor het oogsten van osmotisch vermogen (update)
- Mechanistische basis van zuurstofgevoeligheid in titanium

- Machine learning-software voorspelt gedrag van bacteriën
- Nieuw proces versnelt medicamenteuze behandelingen voor virale infecties en kanker

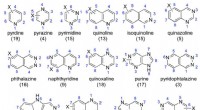
- Naar een beter begrip van structuur-metabolismerelaties in humaan aldehydeoxidase (update)
 Hoe het gebied van een driehoek te vinden op zijn hoekpunten
Hoe het gebied van een driehoek te vinden op zijn hoekpunten  Test van Marsgebonden instrumenten in het Zwarte Woud
Test van Marsgebonden instrumenten in het Zwarte Woud Klimaatmodellen overschatten natuurlijke variabiliteit
Klimaatmodellen overschatten natuurlijke variabiliteit Hoge verwachtingen nu de nieuwe nachttrein van Oostenrijk vertrekt naar Brussel
Hoge verwachtingen nu de nieuwe nachttrein van Oostenrijk vertrekt naar Brussel Tweerichtingssignalering mogelijk met een enkel kwantumdeeltje
Tweerichtingssignalering mogelijk met een enkel kwantumdeeltje Sociaal psycholoog biedt sleutel tot het beëindigen van racisme
Sociaal psycholoog biedt sleutel tot het beëindigen van racisme Wat oude mest onthult over epipaleolithische verzorging van dieren?
Wat oude mest onthult over epipaleolithische verzorging van dieren?  Hoe voorkomen katoenen ballen dat een ei wordt verbroken?
Hoe voorkomen katoenen ballen dat een ei wordt verbroken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


