
Wetenschap
Hoeveel mol ionen worden er geproduceerd als 2 mol Na2CO3 dissocieert?
```
Na2CO3 (water) → 2 Na+ (water) + CO32- (water)
```
Uit deze vergelijking kunnen we zien dat voor elke mol Na2CO3 die dissocieert, er 2 mol Na+-ionen en 1 mol CO32--ionen worden geproduceerd. Daarom kunnen we, als 2 mol Na2CO3 dissocieert, het totale aantal geproduceerde mol ionen als volgt berekenen:
Totaal aantal mol ionen =(2 mol Na2CO3) × (2 mol Na+-ionen/1 mol Na2CO3) + (2 mol Na2CO3) × (1 mol CO32-ionen/1 mol Na2CO3)
Totaal aantal mol ionen =4 mol Na+-ionen + 2 mol CO32-ionen
Totaal aantal mol ionen =6 mol ionen
Wanneer 2 mol Na2CO3 dissocieert, worden er dus in totaal 6 mol ionen (4 mol Na+-ionen en 2 mol CO32-ionen) geproduceerd.
 Wat beïnvloedt de atoomstraal?
Wat beïnvloedt de atoomstraal?  Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën
Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën Loodhalogenide perovskieten:een paard met een andere kleur
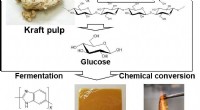
Loodhalogenide perovskieten:een paard met een andere kleur Een glucosevloeistof maken
Een glucosevloeistof maken Wetenschappers ontwikkelen betere manier om virussen te blokkeren die luchtweginfecties bij kinderen veroorzaken
Wetenschappers ontwikkelen betere manier om virussen te blokkeren die luchtweginfecties bij kinderen veroorzaken
 Orkaan Dorian veroorzaakt enorme overstromingen over Bahama's
Orkaan Dorian veroorzaakt enorme overstromingen over Bahama's Wat gebeurt er als je een roofdier opnieuw in een beschermd gebied introduceert? Deze quolls kregen de taak
Wat gebeurt er als je een roofdier opnieuw in een beschermd gebied introduceert? Deze quolls kregen de taak  Hoe cranberrymoerassen werken
Hoe cranberrymoerassen werken  Tot 38 procent van alle jaarlijkse astmagevallen bij kinderen in Bradford kan worden veroorzaakt door luchtvervuiling
Tot 38 procent van alle jaarlijkse astmagevallen bij kinderen in Bradford kan worden veroorzaakt door luchtvervuiling NASA vindt windschering die tropische cycloon Cebile verscheurt
NASA vindt windschering die tropische cycloon Cebile verscheurt
Hoofdlijnen
- Denken dieren rationeel? Onderzoeker suggereert dat voor rationele besluitvorming geen taal nodig is
- Computersimulaties geven aanwijzingen over hoe cellen omgaan met hun omgeving
- Onderzoekers willen weten waarom beluga-walvissen nog niet zijn hersteld
- Gemuteerd kikkergen stoot roofdieren af
- Hoe origami ziektediagnoses kan bepalen
- Team ontdekt hoe microsporidiaanse parasieten sprinkhanenzwermgedrag voorkomen
- In de stad levende pimpelmezen kunnen grotere eieren leggen vanwege wat ze eten
- Onderzoeksteam introduceert vooruitgang in automatische boskarteringstechnologie
- Wat is de chemische formule van creatinekinase?
- Metalen organische kaders metalen meesterschap

- Het opruimen van Tsjernobyl kan worden geholpen door een nieuwe benadering voor röntgenanalyse

- Onderzoek onthult meer over het pad dat bacteriële ziekteverwekkers afleggen om tuberculose te veroorzaken

- Ontwerpen van hiërarchische nanoporeuze membranen voor zeer efficiënte adsorptie- en opslagtoepassingen

- De hoogste hittebestendige kunststof ooit is ontwikkeld uit biomassa
 De grote les uit eerdere pandemieën? Vermijd paniekaankopen, zegt nieuw onderzoek
De grote les uit eerdere pandemieën? Vermijd paniekaankopen, zegt nieuw onderzoek  Enorme concessies bedreigen het Maleisische bos:rapport
Enorme concessies bedreigen het Maleisische bos:rapport  Zal een Samsung-headset binnenkomen op Apples AR-parade?
Zal een Samsung-headset binnenkomen op Apples AR-parade? Trainingstool helpt werkloze werkzoekenden hun netwerkvaardigheden te vergroten
Trainingstool helpt werkloze werkzoekenden hun netwerkvaardigheden te vergroten IJs bevestigd op de maanpolen
IJs bevestigd op de maanpolen Hoe een duiventrap Door
Hoe een duiventrap Door orkanen, overstromingsverzekering en de gevaren van business as usual
orkanen, overstromingsverzekering en de gevaren van business as usual Gaspluimen van Kīlauea onthullen verborgen gevaren van vulkanische vervuiling
Gaspluimen van Kīlauea onthullen verborgen gevaren van vulkanische vervuiling
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

