
Wetenschap
Hoe antivrieseiwitten ijskoud stoppen
De structuur van AFP's varieert afhankelijk van het organisme dat ze produceert. Ze hebben echter allemaal een gemeenschappelijk kenmerk:ze bevatten een groot aantal hydrofiele (waterminnende) aminozuren. Deze aminozuren helpen de AFP's zich te binden aan het oppervlak van ijskristallen.
Wanneer een AFP zich aan een ijskristal bindt, verandert het de vorm van het kristal. Dit maakt het moeilijker voor het kristal om groter te worden. Bovendien kunnen de AFP's ook de vorming van nieuwe ijskristallen remmen.
Het vermogen van AFP's om de groei van ijskristallen te remmen is essentieel voor het voortbestaan van veel organismen. Vissen die in koud water leven zouden bijvoorbeeld niet kunnen overleven zonder AFP's. De AFP's in hun bloed voorkomen dat ze vastvriezen als de watertemperatuur daalt.
AFP's worden ook gebruikt in een verscheidenheid aan commerciële toepassingen. Ze worden bijvoorbeeld gebruikt in antivries voor auto's en vliegtuigen. Ze worden ook gebruikt in diepvriesproducten om de vorming van ijskristallen te voorkomen.
Het onderzoek naar AFP's is nog steeds aan de gang. Wetenschappers proberen te begrijpen hoe AFP's werken en hoe ze kunnen worden gebruikt om de menselijke gezondheid en technologie te verbeteren.
 Innovatieve biogebaseerde luchtfilter kan luchtfiltratie transformeren, mogelijk allergenen in de lucht binnenshuis verminderen
Innovatieve biogebaseerde luchtfilter kan luchtfiltratie transformeren, mogelijk allergenen in de lucht binnenshuis verminderen Onderzoekers ontwikkelen een nieuw type synthetische moleculaire machine
Onderzoekers ontwikkelen een nieuw type synthetische moleculaire machine Nieuwe ontwikkelingen voor het verminderen van defecten in multimaterialen met behulp van gerichte energiedepositie
Nieuwe ontwikkelingen voor het verminderen van defecten in multimaterialen met behulp van gerichte energiedepositie Wat zijn subscripts in een chemische formule die wordt gebruikt om aan te geven?
Wat zijn subscripts in een chemische formule die wordt gebruikt om aan te geven?  Onderzoek stelt een modulaire maatwerkstrategie voor voor defectvrije MOF-scheidingsmembranen
Onderzoek stelt een modulaire maatwerkstrategie voor voor defectvrije MOF-scheidingsmembranen
 Kan iets naar zonneschijn ruiken?
Kan iets naar zonneschijn ruiken?  Klimaatverandering:Engeland moet zich aanpassen of sterven, agentschap waarschuwt
Klimaatverandering:Engeland moet zich aanpassen of sterven, agentschap waarschuwt Waarom wetenschappers koraalrifgegevens moeten openen om habitats te beschermen
Waarom wetenschappers koraalrifgegevens moeten openen om habitats te beschermen Kaarten markeren steden in Michigan, groepen die het zwaarst zullen lijden onder de gevolgen van klimaatverandering
Kaarten markeren steden in Michigan, groepen die het zwaarst zullen lijden onder de gevolgen van klimaatverandering Miami Beachs laatste straatgevecht:wie wordt overspoeld door het overstromingswater?
Miami Beachs laatste straatgevecht:wie wordt overspoeld door het overstromingswater?
Hoofdlijnen
- Onderzoekers verwachten dat nieuwe vispassage de trekvispopulaties zal herstellen
- Nieuwe sorghumcultivars kunnen duizenden liters ethanol produceren
- Wil je tijgers redden? Je kunt maar beter je cijfers op een rij hebben
- Wetenschappers ontwikkelen nieuwe aanpak om belangrijke onontdekte functies van eiwitten te identificeren
- Maki-darm is niet één ecosysteem, het zijn er veel
- Ruimte-indringers:Radiata-dennen verspreiden zich meer in NZ dan eerder werd gedacht
- De opname van koolstof in bossen wordt aangetast door klimaatverandering, suggereert onderzoek naar bladtemperatuur
- Er is dringend behoefte aan een oplossing voor een maas in de houtkap in het voorgestelde Great Koala National Park
- Geautomatiseerde biologie, of hoe je een populatie cellen kunt besturen met een computer
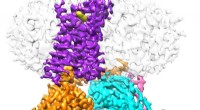
- Dopaminereceptoren in hun oorspronkelijke habitat bekijken
- Nieuwe milieuvriendelijke synthesemethode maakt gebruik van aluminiumoxide als recyclebare katalysator

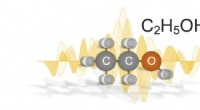
- Alcoholen vertonen kwantumeffecten
- Video:Waarom je geen verse olijven kunt kopen

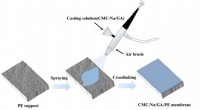
- Pervaporatiemembranen zijn veelbelovend voor de terugwinning van alkalisch afvalwater
 Sommige vissen kunnen van geslacht veranderen op volwassen leeftijd - Heres Why
Sommige vissen kunnen van geslacht veranderen op volwassen leeftijd - Heres Why  Voel de zonsverduistering met NASA's Eclipse Soundscapes-project
Voel de zonsverduistering met NASA's Eclipse Soundscapes-project  De luchtkwaliteit op veel treinstations is alarmerend slecht. Hier leest u hoe u deze kunt verbeteren
De luchtkwaliteit op veel treinstations is alarmerend slecht. Hier leest u hoe u deze kunt verbeteren  China verleent gamelicentie aan NetEase, eerste sinds hardhandig optreden
China verleent gamelicentie aan NetEase, eerste sinds hardhandig optreden Cloudgaming staat voor uitdagingen nu Google de lancering voorbereidt
Cloudgaming staat voor uitdagingen nu Google de lancering voorbereidt Exacte klimaatgegevens uit het verleden
Exacte klimaatgegevens uit het verleden Door na te bootsen hoe de biologische wereld zich inricht, kan de volgende generatie nanomaterialen vooruitgaan
Door na te bootsen hoe de biologische wereld zich inricht, kan de volgende generatie nanomaterialen vooruitgaan Wat als een man anticonceptiepillen slikt?
Wat als een man anticonceptiepillen slikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

