
Wetenschap
Beantwoording van het mysterie van wat atomen doen als vloeistoffen en gassen elkaar ontmoeten
Wanneer een vloeistof en een gas elkaar ontmoeten, beginnen de gasmoleculen in de vloeistof op te lossen. Dit proces wordt ontbinding genoemd. De oplossnelheid zal afhangen van verschillende factoren, waaronder de temperatuur, druk en oppervlakte van de vloeistof.
Temperatuur
Hoe hoger de temperatuur, hoe meer gasmoleculen in de vloeistof oplossen. Dit komt omdat hoe hoger de temperatuur, hoe meer energie de gasmoleculen hebben, en hoe waarschijnlijker het is dat ze de krachten overwinnen die ze bij elkaar houden.
Druk
Hoe hoger de druk, hoe meer gasmoleculen in de vloeistof oplossen. Dit komt omdat hoe hoger de druk, hoe meer gasmoleculen in contact worden gebracht met de vloeistof, en hoe waarschijnlijker het is dat ze oplossen.
Oppervlak van de vloeistof
Hoe groter het oppervlak van de vloeistof, hoe meer gasmoleculen erin zullen oplossen. Dit komt omdat hoe groter het oppervlak is, hoe meer gasmoleculen in contact komen met de vloeistof en hoe waarschijnlijker het is dat ze oplossen.
Wat zijn de gevolgen van ontbinding?
Het oplossen van gasmoleculen in een vloeistof kan een aantal effecten hebben, waaronder:
* Vermindering van de oppervlaktespanning van de vloeistof. Hierdoor kan de vloeistof zich gemakkelijker verspreiden en belletjes vormen.
* De dichtheid van de vloeistof veranderen. Hierdoor kan de vloeistof een grotere of kleinere dichtheid krijgen, afhankelijk van het feit of de gasmoleculen zwaarder of lichter zijn dan de vloeibare moleculen.
* De viscositeit van de vloeistof veranderen. Hierdoor kan de vloeistof meer of minder stroperig worden, afhankelijk van of de gasmoleculen groter of kleiner zijn dan de vloeistofmoleculen.
* De kleur van de vloeistof veranderen. Dit kan gebeuren als de gasmoleculen licht van een bepaalde kleur absorberen of reflecteren.
Verzoek tot ontbinding
Het oplossen van gasmoleculen in vloeistoffen kent een aantal belangrijke toepassingen, waaronder:
* Koolzuurhoudende dranken. Het kooldioxidegas dat koolzuurhoudende dranken hun bruisende smaak geeft, wordt onder druk in de vloeistof opgelost.
* Duiken. Duikers gebruiken perslucht, een mengsel van zuurstof- en stikstofgassen, om onder water te ademen. Het stikstofgas wordt opgelost in het bloed van de duiker en komt vrij wanneer de duiker aan de oppervlakte komt.
* Brandbestrijding. Brandweerlieden gebruiken water om branden te blussen. Het water absorbeert de warmte van het vuur en de geproduceerde stoom helpt de vlammen te doven.
* Chemische reacties. Veel chemische reacties vinden plaats in oplossing, waarbij de reactanten in een vloeistof worden opgelost. Hierdoor kunnen de reactanten gemakkelijker met elkaar in contact komen en wordt de reactie versneld.
 Synchrotron-straling werpt licht op het vormingsmechanisme van aromatische polyimide-precursor
Synchrotron-straling werpt licht op het vormingsmechanisme van aromatische polyimide-precursor Niezen cam onthult de beste stoffencombinaties voor stoffen maskers
Niezen cam onthult de beste stoffencombinaties voor stoffen maskers AI-simulatie van gearomatiseerde dampreacties onthult de vorming van veel gevaarlijke chemicaliën
AI-simulatie van gearomatiseerde dampreacties onthult de vorming van veel gevaarlijke chemicaliën  Zwaveldioxide transformeren van schadelijk naar nuttig
Zwaveldioxide transformeren van schadelijk naar nuttig Hoe wordt het bos beïnvloed door zure regen?
Hoe wordt het bos beïnvloed door zure regen?
 Uit onderzoek blijkt hoe het plantenwelzijn wordt verbeterd door schimmels in de bodem
Uit onderzoek blijkt hoe het plantenwelzijn wordt verbeterd door schimmels in de bodem  Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?
Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?  Burgerwetenschap voor duurzame ontwikkeling
Burgerwetenschap voor duurzame ontwikkeling Naarmate het klimaat het Arctische zee-ijs sneller opschudt, vervuilingstags mee
Naarmate het klimaat het Arctische zee-ijs sneller opschudt, vervuilingstags mee Grote bedrijven zullen binnenkort hun klimaatrisico bekend moeten maken, maar zal het helpen?
Grote bedrijven zullen binnenkort hun klimaatrisico bekend moeten maken, maar zal het helpen?
Hoofdlijnen
- Voelen planten pijn?
- Neurale opnames van wilde vleermuizen onthullen een unieke organisatie van het middenhersenengebied voor het volgen en vangen van prooien
- Hoe maak je een 3-D DNA-model voor High School Biology
- Organellen gevonden in beide planten- en bacteriecellen
- Van dichtbij en persoonlijk tonen krekels de kunstwerken van de natuur. Opmerkzame toeschouwers vinden schoonheid in insecten.
- Afbrekende koraalriffen slecht nieuws voor commerciële visserij
- De voordelen van Stained Bacteria
- Waarom zijn er 61 Anticodonen?
- Nieuwe studie ontdekt hoe veranderde eiwitvouwing de meercellige evolutie aandrijft
- Celfabriek die zeer zuiver DHA kan produceren
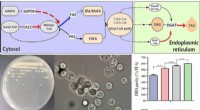
- Verdunning detecteren:nieuwe experimentele en theoretische benaderingen duiken in de pool van organellen van membranen

- Elektrolytisch gespoten microdruppeltjes helpen bacteriën en virussen te doden

- De eigenschappen van composieten voor het bouwen van betrouwbare treinen

- Laserdiode detecteert valse olijfolie

 Gratis en voedzame schoollunches helpen om rijkere en gezondere volwassenen te creëren
Gratis en voedzame schoollunches helpen om rijkere en gezondere volwassenen te creëren Nieuw computermodel automatisch, foto's esthetisch bijsnijden
Nieuw computermodel automatisch, foto's esthetisch bijsnijden Donkere inflatie opent een zwaartekrachtvenster op de eerste momenten na de oerknal
Donkere inflatie opent een zwaartekrachtvenster op de eerste momenten na de oerknal Koolstofproductiviteit:wat als we het belangrijkste zouden meten?
Koolstofproductiviteit:wat als we het belangrijkste zouden meten? De weg vrijmaken voor de herdefiniëring van de eenheid van temperatuur
De weg vrijmaken voor de herdefiniëring van de eenheid van temperatuur Scholieren reageren vooral op één of twee buren tegelijk
Scholieren reageren vooral op één of twee buren tegelijk Spin-golfcircuits op nanoschaal gebaseerd op geconstrueerde herconfigureerbare spin-texturen
Spin-golfcircuits op nanoschaal gebaseerd op geconstrueerde herconfigureerbare spin-texturen Het onzichtbare zien:hoe vlinders wetenschappers kunnen helpen kanker op te sporen
Het onzichtbare zien:hoe vlinders wetenschappers kunnen helpen kanker op te sporen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

