
Wetenschap
Vooruitgang in de biosynthese van taxol zou kunnen leiden tot grootschalige productie van geneesmiddelen tegen kanker
Paclitaxel is 's werelds best verkochte plantaardige kankermedicijn en een van de meest effectieve kankermedicijnen van de afgelopen 30 jaar. Het wordt veel gebruikt bij de behandeling van verschillende soorten kanker, waaronder borstkanker, longkanker en eierstokkanker.
Aan het eind van de jaren negentig en het begin van de 21e eeuw bedroeg de jaarlijkse verkoop van paclitaxel meer dan $1,5 miljard en bedroeg in 2001 $2,0 miljard, waarmee het in 2001 het best verkochte medicijn was. In 2019 bedroeg de markt voor paclitaxel en zijn derivaten ongeveer $15 miljard, en Er wordt verwacht dat dit in 2025 20 miljard dollar zal bedragen.
Als geneesmiddel tegen kanker is de moleculaire structuur van paclitaxel uiterst complex, met sterk geoxideerde, ingewikkelde overbrugde ringen en 11 stereocentra, waardoor het algemeen wordt erkend als een van de meest uitdagende natuurlijke producten om chemisch te synthetiseren. Sinds de eerste totale synthese van paclitaxel werd gerapporteerd door de onderzoeksgroepen van Holton en Nicolaou in 1994, zijn meer dan 40 onderzoeksteams betrokken geweest bij de totale synthese van paclitaxel.
Maar zelfs bij de kortste chemische syntheseroute tot nu toe bedraagt de totale opbrengst aan paclitaxel slechts 0,118%, wat niet voldoende is om aan de vraag naar industriële productie te voldoen. Momenteel maakt de industriële productie van paclitaxel gebruik van een semi-synthetische strategie:het isoleren van voorlopers van paclitaxel (zoals baccatine III) uit plantencelculturen of Taxus-bladeren en deze vervolgens via chemische methoden omzetten in paclitaxel. De semi-synthetische strategie is echter sterk afhankelijk van natuurlijke hulpbronnen en wordt beperkt door de langzame groei van Taxus-cellen of -bladeren, en kan dus niet voldoen aan de groeiende marktvraag.
Met de snelle ontwikkeling van de biotechnologie zijn synthetische biologiestrategieën voor de microbiële biosynthese van plantaardige natuurlijke producten naar voren gekomen als een krachtige aanpak voor het efficiënt produceren van complexe plantaardige natuurlijke producten.
Daarom heeft het bereiken van een efficiënte, milieuvriendelijke en duurzame productie van paclitaxel door middel van synthetische biologie brede aandacht getrokken. Het realiseren van de de novo synthese van paclitaxel in een heteroloog systeem vereist echter het identificeren van de belangrijkste enzymen die ontbreken in de biosyntheseroute van paclitaxel en het vaststellen van een volledige biosyntheseroute voor paclitaxel.
Om de al lang bestaande uitdaging van de biosynthese van paclitaxel in Taxus aan te pakken, hebben twee onderzoeksteams onder leiding van prof. Jianbin Yan (Agricultural Genomics Institute in Shenzhen, AGIS) en prof. Xiaoguang Lei (Peking University, PKU), evenals andere onderzoeksteams van vijf andere verschillende instellingen, waaronder Tsinghua University en UCLA, hebben samengewerkt om met succes de ontbrekende enzymen te identificeren en de reconstructie van de biosynthetische enzymen te bewerkstelligen die tot baccatine III leiden.
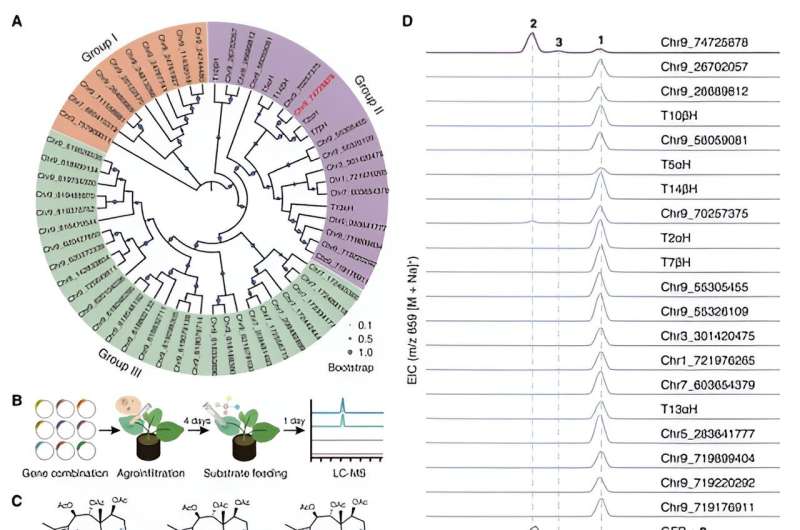
De onderzoekers gebruikten een heteroloog expressiesysteem voor tabak om activiteitsscreening uit te voeren van de CYP725A-genfamilie die specifiek in Taxus wordt aangetroffen via substraat-co-injectiestrategie. Ze hebben met succes een biosynthetisch enzym geïdentificeerd, genaamd Taxane oxetanase (TOT), dat de vorming van de oxetaanring katalyseert tijdens de biosyntheseroute van taxol.
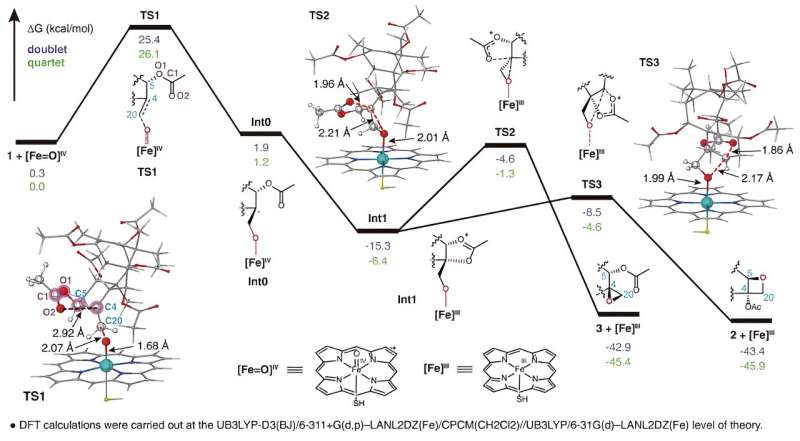
TOT katalyseert de vorming van de unieke oxetaanring door oxidatie van de dubbele C4,20-binding en daaropvolgende herschikking van de aangrenzende acetylgroep op de C5-positie, zoals weergegeven in. Dit nieuwe reactiemechanisme van de vorming van oxetaanringen doorbreekt het conventionele begrip dat oxetaanringen vorming in de biosyntheseroute van taxol wordt bereikt door een herschikkingsreactie van het overeenkomstige epoxide.
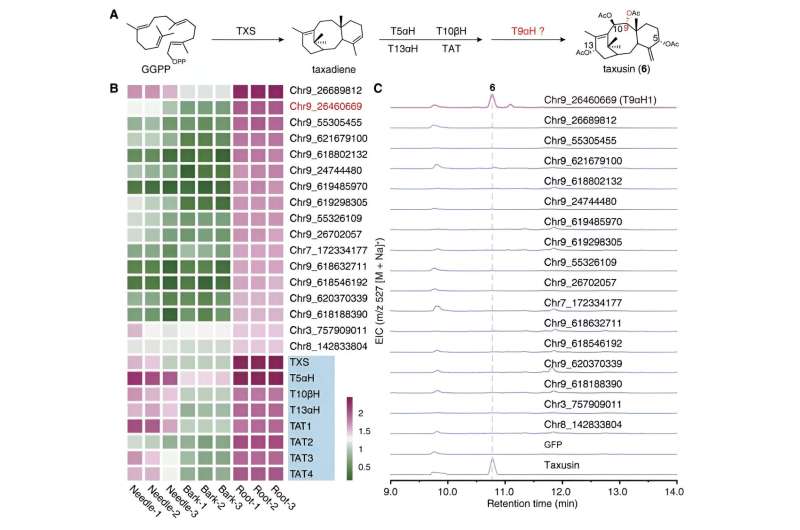
Door zich te concentreren op de structureel eenvoudiger verbinding, taxusine, identificeerden de onderzoekers 17 kandidaatgenen die coderen voor enzymen die verantwoordelijk zijn voor de C9-oxidatie van taxanen met behulp van de co-expressieanalyse en metabolismeanalyse. Deze kandidaat-genen werden verder onderworpen aan activiteitsscreening door de biosyntheseroute van taxusine in tabak te reconstrueren, wat leidde tot de ontdekking van het enzym dat verantwoordelijk is voor C9-oxidatie in taxanen, genaamd Taxane 9α-hydroxylase (T9αH).
Met deze twee nieuw geïdentificeerde enzymen TOT en T9αH in handen probeerden onderzoekers de totale biosynthese van baccatine III in tabak te bereiken door deze samen tot expressie te brengen met andere bekende biosynthetische genen van taxol. Ze hebben met succes de productie van baccatine III in tabak gedetecteerd wanneer TOT en T9αH tot co-expressie werden gebracht met andere zeven bekende biosynthetische genen (TXS, T5αH, T13αH, T2αH, T7βH, TAT en TBT). Bovendien hebben ze aangetoond dat deze negen genen de kerngenen zijn voor de biosynthese van baccatine III, aangezien elk gen onmisbaar is voor de biosynthese van baccatine III in tabak.
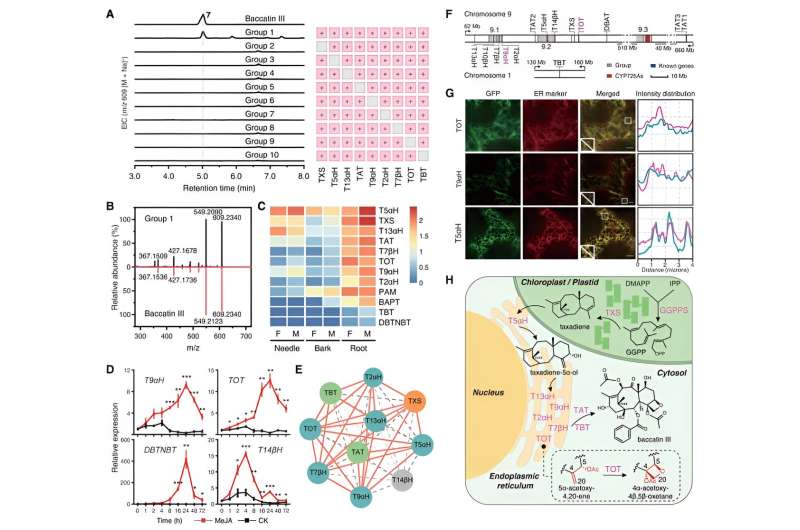
Verdere biochemische onderzoeken hebben aangetoond dat deze kerngenen een nauwe functionele synergie vertonen en mede worden gereguleerd door het plantenhormoon jasmonaat, wat vergelijkbare inductie-expressiepatronen en sterke expressiecorrelatie aantoont. Door subcellulaire lokalisatieanalyse en andere experimentele resultaten te combineren, bieden onderzoekers een compleet overzicht van het biosyntheseproces van baccatine III.
Het uitgangssubstraat GGPP wordt door TXS gekatalyseerd om taxadieen in chloroplasten te vormen. Vervolgens wordt taxadieen overgebracht naar het cytoplasma via de contactplaatsen van het plastide-endoplasmatisch reticulum en ondergaat het gecoördineerde katalyse door zes membraangebonden oxidasen (T2αH, T5αH, T7βH, T9αH, T13αH en TOT) verankerd in het endoplasmatisch reticulum en twee cytoplasmatische acyloxidasen. transferasen (TAT en TBT), wat uiteindelijk resulteert in de vorming van baccatine III.
Samenvattend is dit onderzoek, gepubliceerd in Science combineert onlangs meerdere omics-analyses en uitgebreide functionele validatie om met succes de belangrijkste ontbrekende enzymen in de biosyntheseroute van paclitaxel te identificeren. Het onthult een nieuw mechanisme waarmee plantencellen de vorming van oxetaanringen katalyseren en ontdekt de kortste route voor de heterologe biosynthese van paclitaxel.
Door negen kernenzymen in tabak tot co-expressie te brengen, bereiken de onderzoekers de bioproductie van de voorloper van paclitaxel, baccatine III, waardoor de basis wordt gelegd voor de grootschalige productie van paclitaxel en ook theoretische begeleiding wordt geboden voor biosynthetische onderzoeken naar honderden andere natuurlijke taxaanproducten.
Meer informatie: Bin Jiang et al, Karakterisering en heterologe reconstitutie van biosynthetische Taxus-enzymen leidend tot baccatine III, Wetenschap (2024). DOI:10.1126/science.adj3484
Journaalinformatie: Wetenschap
Aangeboden door de Universiteit van Peking
 Onderzoekers ontdekken de boosdoeners achter putcorrosie in 3D-geprint roestvrij staal
Onderzoekers ontdekken de boosdoeners achter putcorrosie in 3D-geprint roestvrij staal  Katalysatoren zoals een pincet gebruiken om één enantiomeer uit een gespiegeld paar te selecteren
Katalysatoren zoals een pincet gebruiken om één enantiomeer uit een gespiegeld paar te selecteren Van orkanen tot aardbevingen, ruimtestation experiment overwint uitdagingen
Van orkanen tot aardbevingen, ruimtestation experiment overwint uitdagingen Onderzoekers ontdekken spontane vloeibaarmaking van grensvlakken tussen vast metaal en vloeibaar metaal in colloïdale binaire legeringen
Onderzoekers ontdekken spontane vloeibaarmaking van grensvlakken tussen vast metaal en vloeibaar metaal in colloïdale binaire legeringen  Bufferoplossingen voorbereiden
Bufferoplossingen voorbereiden
 NASA kijkt naar waterdamp in tyfoon Soulik
NASA kijkt naar waterdamp in tyfoon Soulik In Nigeria vervuild Ogoniland, tekenen van een opruiming
In Nigeria vervuild Ogoniland, tekenen van een opruiming Interdisciplinaire benadering de enige manier om de verwoestende effecten van bodemerosie aan te pakken
Interdisciplinaire benadering de enige manier om de verwoestende effecten van bodemerosie aan te pakken NASA/JAXA-satelliet vindt zware regenval in tropische storm Isaac
NASA/JAXA-satelliet vindt zware regenval in tropische storm Isaac Warmte opgesloten in stedelijke gebieden laat bomen denken dat de lente eerder is aangebroken
Warmte opgesloten in stedelijke gebieden laat bomen denken dat de lente eerder is aangebroken
Hoofdlijnen
- Differentiërende RNA & DNA-virussen
- De chemische stof die planten vertelt wanneer het tijd is om te slapen
- De positieve effecten van genetische manipulatie
- Onderzoekers ontdekken dat stress tijdens de zwangerschap de grootte van de baby beïnvloedt
- Hoe wordt een bij een bijenkoningin?
- Groene Brexit laten werken voor landbouw en milieu
- Verdediging tegen bijna elke prijs
- Wat veroorzaakte de enorme kiespijn van deze megatandhaai?
- Hoe inheemse, bedreigde vogels te beschermen tegen zonne-installaties in Hawaï
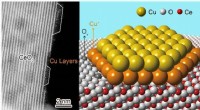
- Wetenschappers identificeren atomaire structuur van katalytisch actieve koper-ceriumoxide-interface
- Geleidende aard in kristalstructuren onthuld bij een vergroting van 10 miljoen keer

- Kristaleilanden kunnen de tijd en kosten van wetenschappelijke experimenten halveren

- Macromoleculaire kristallografie werpt licht op een nieuwe manier om de malariaparasiet aan te pakken

- Een materiaal met een bijzondere twist:2-D molybdeendiselenidekristal

 Met stijgende zeespiegels, Bangkok worstelt om overeind te blijven
Met stijgende zeespiegels, Bangkok worstelt om overeind te blijven Waarom AI-robotspeelgoed goed kan zijn voor kinderen
Waarom AI-robotspeelgoed goed kan zijn voor kinderen Nieuwe studie verklaart de koudste temperaturen van Antarctica
Nieuwe studie verklaart de koudste temperaturen van Antarctica Rechters wegen $ 8,5 miljoen schikking met $ 0 tot 129 miljoen Google-gebruikers
Rechters wegen $ 8,5 miljoen schikking met $ 0 tot 129 miljoen Google-gebruikers Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan
Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan Een natuurlijk tintje voor kustverdediging:hybride oplossingen kunnen meer voordelen bieden in gebieden met een lager risico
Een natuurlijk tintje voor kustverdediging:hybride oplossingen kunnen meer voordelen bieden in gebieden met een lager risico  Een nieuw plan om de oudste ontdekkingsreizigers van NASA op de been te houden
Een nieuw plan om de oudste ontdekkingsreizigers van NASA op de been te houden Een zeldzaam natuurverschijnsel zorgt voor ernstige droogte in Australië. Door klimaatverandering komt het vaker voor
Een zeldzaam natuurverschijnsel zorgt voor ernstige droogte in Australië. Door klimaatverandering komt het vaker voor
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

