
Wetenschap
Nieuw soort interactie ontdekt in waterstofproducerende enzymen

Krediet:Pixabay/CC0 publiek domein
Hydrogenasen kunnen waterstof net zo efficiënt omzetten als dure platinakatalysatoren. Om ze bruikbaar te maken voor biotechnologische toepassingen, onderzoekers ontcijferen tot in detail hoe ze werken. Een team van Ruhr-Universität Bochum en de Universiteit van Oxford rapporteert nu in het tijdschrift Proceedings van de National Academy of Sciences ( PNAS ) dat de overdracht van protonen en elektronen door het enzym ruimtelijk gescheiden plaatsvindt, maar is toch gekoppeld en dus, een beslissende factor voor efficiëntie. Het artikel is online gepubliceerd op 10 augustus 2020.
Meest efficiënte waterstofproducenten
De zogenaamde klasse van [FeFe]-hydrogenasen, die bijvoorbeeld voorkomen in groene algen, zijn de meest efficiënte waterstofproducenten van de natuur. Ze kunnen zowel waterstof produceren als splitsen. De eigenlijke chemische reactie vindt plaats op de actieve plaats die diep in het enzym is begraven. "De elektronen en protonen die nodig zijn voor de reactie moeten daarom een efficiënte manier vinden om daar te komen, " legt Dr. Oliver Lampret van de Photobiotechnology Research Group in Bochum uit, een van de auteurs van het artikel. Elektronentransport vindt plaats via een elektrische draad, bij wijze van spreken, bestaande uit verschillende ijzer-zwavelclusters. De protonen worden naar het actieve centrum getransporteerd via een protonoverdrachtsroute bestaande uit vijf aminozuren en één watermolecuul.
"Hoewel het bekend was dat er een proton-gekoppeld elektronoverdrachtmechanisme was, onderzoekers gingen er tot nu toe van uit dat de koppeling alleen plaatsvindt in het actieve centrum zelf, " zegt professor Thomas Happe, Hoofd van de onderzoeksgroep fotobiotechnologie.
Eiwitengineering maakt koppeling zichtbaar
Het team manipuleerde de hydrogenasen op zo'n manier dat de overdracht van protonen aanzienlijk langzamer was, maar waterstof kon nog steeds worden omgezet. Met behulp van dynamische elektrochemie, ze toonden aan dat de waterstofconversie aanzienlijk afnam en nog belangrijker, significante overpotentialen waren nodig om de productie of splitsing van waterstof te katalyseren. Door de protonoverdrachtsroute te manipuleren, de onderzoekers hadden indirect de snelheid van elektronenoverdracht verlaagd.
"Omdat de twee overdrachtsroutes ruimtelijk gescheiden zijn, we nemen aan dat een coöperatieve langeafstandskoppeling van beide processen nodig is voor efficiënte katalyse, " concludeert Oliver Lampret. De bevindingen moeten helpen om in de toekomst efficiëntere geminiaturiseerde hydrogenase-katalysatoren te ontwikkelen.
 Een manier om de absolute stereochemie van kleine, organische moleculen
Een manier om de absolute stereochemie van kleine, organische moleculen Doorzeefd met gaten:flexibele dunnefilmelektronica duurzamer maken
Doorzeefd met gaten:flexibele dunnefilmelektronica duurzamer maken Het verschil tussen isotopen van hetzelfde element
Het verschil tussen isotopen van hetzelfde element  Onderzoekers ontwikkelen nieuwe methode om metaal te analyseren
Onderzoekers ontwikkelen nieuwe methode om metaal te analyseren Wat zijn de beperkingen van Covalent & Metallic Roosters?
Wat zijn de beperkingen van Covalent & Metallic Roosters?
Hoofdlijnen
- Zijn psychische aandoeningen genetisch bepaald?
- Secretine-eiwit met een kroon
- Goed excuus,
- Ziekteverwekkers tegen elkaar keren om resistentie tegen geneesmiddelen te voorkomen
- Relatie tussen celstructuur en functie
- Nieuwe oude dolfijnsoort Urkudelphis chawpipacha ontdekt in Ecuador
- Verschil tussen plant- en diercelafdeling
- Het sluiten van wegen gaat de effecten van habitatverlies voor grizzlyberen tegen
- Computersimulaties onthullen wortels van resistentie tegen geneesmiddelen
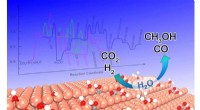
- Water zou de activiteit en selectiviteit van koolstofdioxidereductie kunnen moduleren
- Nieuwe methode voor nauwkeurigere bepaling van het tijdstip van overlijden op plaats delict

- Eencellige test kan precies onthullen hoe medicijnen kankercellen doden

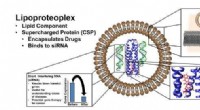
- Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert
- Onderzoekers gebruiken drukgevoelige moleculaire materialen om koeltechnologie te benutten

 NASA luidt het nieuwe jaar in met historische flyby van verre wereld
NASA luidt het nieuwe jaar in met historische flyby van verre wereld Bossen spelen belangrijke rol bij het halen van de klimaatdoelstellingen van Parijs
Bossen spelen belangrijke rol bij het halen van de klimaatdoelstellingen van Parijs Astronomen ontdekken krachtige kosmische dubbele klap
Astronomen ontdekken krachtige kosmische dubbele klap Hoe lang duurt het voordat een zonnevlam de aarde bereikt?
Hoe lang duurt het voordat een zonnevlam de aarde bereikt?  Asteroïde-monster dat naar de aarde is teruggebracht, wordt van dichtbij bekeken
Asteroïde-monster dat naar de aarde is teruggebracht, wordt van dichtbij bekeken Hoe middelbare scholen dieper leren kunnen bevorderen
Hoe middelbare scholen dieper leren kunnen bevorderen Nieuwe tests kunnen kleine maar giftige deeltjes koolas in de bodem detecteren
Nieuwe tests kunnen kleine maar giftige deeltjes koolas in de bodem detecteren Marineonderzoekers rekruteren lichtgevende nanodeeltjes om de hersenfunctie in beeld te brengen
Marineonderzoekers rekruteren lichtgevende nanodeeltjes om de hersenfunctie in beeld te brengen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

