
Wetenschap
Hoe bouwen bacteriën natuurlijke producten op?
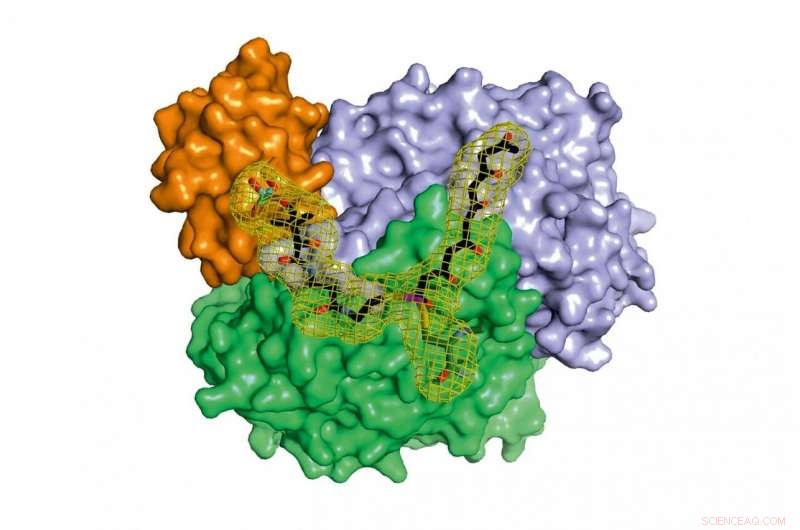
Een complex van drie eiwitten beschermt het zeer reactieve hexaketide wanneer het wordt uitgebreid tot het octaketide. In samenwerking met andere eiwitten, Uit het resulterende octaketide worden belangrijke natuurlijke stoffen geproduceerd. Credit:Maximilian Schmalhofer en Prof. Dr. Michael Groll/TUM
De werkzame stoffen van veel medicijnen zijn natuurlijke producten, zo genoemd omdat vaak alleen micro-organismen in staat zijn om de complexe structuren te produceren. Vergelijkbaar met de productielijn in een fabriek, grote enzymcomplexen brengen deze actieve stofmoleculen samen. Een team van de Technische Universiteit van München (TUM) en de Goethe Universiteit Frankfurt is er nu in geslaagd om de basismechanismen van een van deze moleculaire fabrieken te onderzoeken.
Veel belangrijke medicijnen zoals antibiotica of actieve middelen tegen kanker zijn natuurlijke producten die worden opgebouwd door micro-organismen, bijvoorbeeld bacteriën of schimmels. In het laboratorium, deze natuurlijke producten zijn vaak niet of slechts met veel moeite te maken. Het startpunt van een groot aantal van dergelijke verbindingen zijn polyketiden, dat zijn koolstofketens waar elk tweede atoom een dubbele binding heeft met een zuurstofatoom.
In een microbiële cel zoals in de Photorhabdus luminescens bacterie, ze worden geproduceerd met behulp van polyketidesynthasen (PKS). Om stap voor stap de gewenste moleculen op te bouwen, in de eerste fase van PKS type II-systemen, vier eiwitten werken samen in veranderende 'teams'.
In een tweede fase, ze worden vervolgens door verdere enzymen gemodificeerd tot het gewenste natuurlijke product. Voorbeelden van bacteriële natuurproducten die op die manier worden geproduceerd zijn, onder andere, de klinisch gebruikte tetracycline-antibiotica of doxorubicine, een medicijn tegen kanker.
Interdisciplinaire samenwerking
Hoewel de gewijzigde stappen van de tweede fase goed zijn bestudeerd voor veel actieve middelen, er is tot nu toe nauwelijks inzicht in de algemene werking van de eerste fase van deze moleculaire fabrieken waar het zeer reactieve polyketide-tussenproduct aan het enzymcomplex wordt gebonden en beschermd zodat het niet spontaan kan reageren.
Dit gat wordt nu gedicht door de resultaten van de samenwerking tussen de werkgroepen van Michael Groll, hoogleraar biochemie aan de Technische Universiteit van München, en Helge Bode, hoogleraar moleculaire biotechnologie aan de Goethe-universiteit Frankfurt, die zijn gepubliceerd in het gerenommeerde wetenschappelijke tijdschrift Natuurchemie .
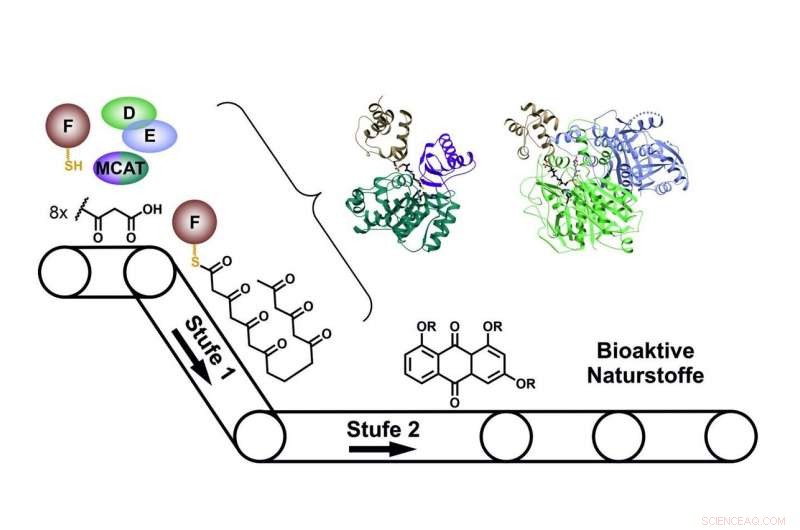
Bij het bouwen van natuurlijke producten werken de individuele enzymen van het Type II PKS-systeem samen als de lopende band van een fabriek. Credit:Prof. Dr. Helge Bode/Goethe-Universitaet Frankfurt
Bevindingen inspireren tot nieuwe syntheses van actieve middelen
"In het kader van dit werk we waren voor het eerst in staat om complexen van de verschillende partnereiwitten van type II polyketidesynthase te analyseren met behulp van röntgenstructuuranalyse en begrijpen nu de volledige katalytische cyclus in detail, " legt Michael Groll uit.
"Op basis van deze bevindingen in de toekomst zal het mogelijk zijn om de centrale biochemische processen gericht te manipuleren en zo de basisstructuren te veranderen in plaats van zich te beperken tot de decorerende enzymen, " voegt Helge Bode toe.
Hoewel het een lange weg is om verbeterde antibiotica en andere medicijnen te ontwikkelen, beide groepen zijn optimistisch dat nu ook de structuur en het mechanisme van de ontbrekende onderdelen van de moleculaire fabriek kan worden verklaard. "We hebben al veelbelovende gegevens van de verdere eiwitcomplexen, " zegt Maximiliaan Schmalhofer, die als promovendus in München bij het onderzoek betrokken was.
 Next-gen 3D-geprinte katalysatoren om hypersonische vlucht voort te stuwen
Next-gen 3D-geprinte katalysatoren om hypersonische vlucht voort te stuwen Gerecycled beton en CO₂ uit de lucht verwerkt tot nieuw bouwmateriaal
Gerecycled beton en CO₂ uit de lucht verwerkt tot nieuw bouwmateriaal Een eencijferige houten luidspreker met een dikte van één micrometer
Een eencijferige houten luidspreker met een dikte van één micrometer Wetenschappers duwen microscopie naar submoleculaire resolutie
Wetenschappers duwen microscopie naar submoleculaire resolutie Een vereenvoudigde methode om olijfolie te categoriseren
Een vereenvoudigde methode om olijfolie te categoriseren
Hoofdlijnen
- Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
- Statistische modellering helpt visserijbeheerders invasieve soorten te verwijderen
- Perfect bewaarde prehistorische leeuwenwelp gevonden in Russische permafrost
- Hoe kunnen nieuwe cellen iemands gezichtsvermogen herstellen?
- Tijger botten? Leeuw botten? Een bijna uitgestorven cycad? DNA-controles ter plaatse bij aankomsthavens
- Wat is een homologe eigenschap?
- Hernieuwde oproepen voor legale jacht om de groeiende berenpopulatie in Connecticuts onder controle te houden
- Hommels bestuderen om meer te leren over menselijke intelligentie en geheugen
- Processen die ATP gebruiken als energiebron
- Meten van kleine krachten die tot grote effecten leiden

- Neutronen brengen atomaire kaart van het virale replicatiemechanisme van COVID-19 in kaart
- Onderzoekers bedenken nieuw proces om suikers uit hout te extraheren

- DNA programmeren om medicijnen tegen kanker af te leveren

- Verrassende ontdekking van spinnenhaar kan leiden tot sterkere lijmen
 Wetenschappers maken zeer transparante zonnecellen voor ramen die elektriciteit opwekken
Wetenschappers maken zeer transparante zonnecellen voor ramen die elektriciteit opwekken What Covers the Moon at Night
What Covers the Moon at Night Hatchet enzym, aanjager van ziekte en gezondheid, blootgesteld door neutronenstralen
Hatchet enzym, aanjager van ziekte en gezondheid, blootgesteld door neutronenstralen Radioactiviteit blijft hangen bij atoombomtests van 1946-1958
Radioactiviteit blijft hangen bij atoombomtests van 1946-1958 De volgende black-out voorkomen
De volgende black-out voorkomen Van veerkracht naar aanpassing:het geval van orkanen
Van veerkracht naar aanpassing:het geval van orkanen Tips voor het oplossen van kwadratische vergelijkingen
Tips voor het oplossen van kwadratische vergelijkingen Een gepoolde standaardfout berekenen
Een gepoolde standaardfout berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

