
Wetenschap
Unieke medicijnstructuren vinden met kunstmatige intelligentie en chemie
Krediet:CC0 Publiek Domein
In de zoektocht naar nieuwe medicijnen tegen ziekten als kanker, een Leids team heeft een nieuwe workflow ontwikkeld. Deze aanpak combineert kunstmatige intelligentie (AI) met moleculaire modellering en is geschikt voor het vinden van onbekende en innovatieve medicijnstructuren, bewezen de onderzoekers.
Doelwit tegen kanker
Met hun nieuwe methode de onderzoekers van het Leiden Academic Centre for Drug Research (LACDR) en het Leiden Institute of Advanced Computer Science (LIACS) konden vijf stoffen vinden met een remmende werking op een bepaald type kinase. Kinasen zijn enzymen die andere eiwitten aan- of uitzetten en een belangrijke rol spelen bij het ontstaan van kanker. In hun publicatie in de Tijdschrift voor chemische informatie en modellering , het team keek naar de zogenaamde polyfarmacologie:de ontwikkeling van geneesmiddelen waarbij er meerdere doelen in het lichaam zijn (zie kader hieronder).
De uitdaging
Het begon in december 2017 met een uitdaging, zegt eerste auteur en Ph.D. kandidaat Lindsey Burggraaff. "Een non-profitorganisatie geleid door Amerikaanse universiteiten en verschillende farmaceutische bedrijven organiseert regelmatig uitdagingen, waaronder deze Multi-targeting Drug DREAM Challenge." De deelnemers kregen de opdracht om moleculen te vinden die aan meerdere kinasen binden. "Er zijn al stoffen gevonden die actief zijn op verschillende kinasen, maar ze lijken allemaal erg op elkaar, ", zegt Burggraaff. "Daarom wilden we nieuwe en originele hits vinden. Deze hits dienen dan als startpunt voor verder drugsonderzoek, als een sjabloon die je kunt optimaliseren."
Een nieuwe strategie
Omdat het team in een beperkte tijd nieuwe en originele moleculen wilde vinden, ze moesten ook een nieuwe strategie bedenken. Burggraaff:"Over het algemeen mensen kiezen voor machine learning of computationele chemie in hun zoektocht naar medicijnen. We argumenteren nu dat het in het geval van polyfarmacologie het beste is om de twee te combineren, zeker als je in korte tijd nieuwe structuren wilt vinden."
De computer trainen
Dit werkt als volgt:Burggraaff en haar afdeling gaven de LIACS-onderzoekers een oefenset, die bekende moleculen en hun eigenschappen bevatten. Met behulp van machinaal leren, de computerwetenschappers konden hun computermodel zo trainen dat het alleen de actieve moleculen uit de set haalde. Voor de uitdaging, datzelfde model pasten ze vervolgens toe op een database van meer dan tien miljoen stoffen. "Dit resulteerde in een kwart miljoen potentieel actieve moleculen. Een effectief eerste filter, ", zegt de promovendus.
Sleutel en slot
Daarna gingen de farmacologen van het LACDR aan de slag met structuurgebaseerd onderzoek. "Het gaat om simulatie van de structuur van je doelwit op de computer, in dit geval, kinase-enzymen, ", zegt Burggraaff. "De computer berekent of het geteste molecuul in het doelwit past, als een sleutel in een slot. Deze methode is veel gedetailleerder dan machine learning, maar neemt ook veel meer tijd in beslag. Daarom werkt de combinatie zo goed."
uiteindelijk, hun inspanningen leverden vijf moleculen op die activiteit vertoonden in laboratoriumtests. “Het bewijs dat onze nieuwe manier van werken nuttig kan zijn. het is niet beperkt tot kinase-onderzoek, het kan ook op grote schaal worden toegepast op andere doelen."
De samenwerking met LIACS stimuleerde de oprichting van het Centre for Computational Life Sciences (CCLS) – een cluster van ongeveer veertig wetenschappers, waaronder onderzoekers van het Instituut Biologie Leiden (IBL), het Mathematisch Instituut (MI), het Leids Instituut voor Chemie (LIC) en het Leids Universitair Medisch Centrum (LUMC). "We spreken de wetenschappers van de afdeling Informatica regelmatig, dus zo is de samenwerking voor deze paper begonnen, ", zegt Burggraaff. Ze noemt het een succesvolle samenwerking. "We hadden maar drie maanden voor deze uitdaging, en veel werk te doen. Dus we hebben elkaar echt gepusht, ', zegt Burggraaff.
"De CCLS is een succesvol voorbeeld van hoe de verschillende klassieke disciplines naar elkaar toe groeien op het snijvlak van de informatica, " zegt Gerard van Westen, laatste auteur. "Met het SAILS-programma op dezelfde manier bundelen we de expertise van alle faculteiten op het gebied van AI, maar dan op het niveau van de hele universiteit. Je ziet dat er op heel verschillende gebieden vergelijkbare uitdagingen zijn die we samen kunnen oplossen." Burggraaff en Van Westen verwachten dat projecten als deze, waarin de expertise van verschillende wetenschappers wordt ingezet voor een concreet doel, leidt tot nieuwe inzichten en innovatieve medicijnen.
 Eiwit dat volledig vanuit het niets is ontworpen, functioneert in cellen als een echt enzym
Eiwit dat volledig vanuit het niets is ontworpen, functioneert in cellen als een echt enzym De sleutel tot het verminderen van de uitstoot van kooldioxide is gemaakt van metaal
De sleutel tot het verminderen van de uitstoot van kooldioxide is gemaakt van metaal Experimentele studie van hoe metallisch glas een uitdaging vormt voor het paradigma in glasonderzoek
Experimentele studie van hoe metallisch glas een uitdaging vormt voor het paradigma in glasonderzoek Onderzoekers produceren 50x stabieler adsorbens
Onderzoekers produceren 50x stabieler adsorbens Verdunningen maken
Verdunningen maken
 Regen is belangrijk voor de invloed van kooldioxide op graslanden
Regen is belangrijk voor de invloed van kooldioxide op graslanden Char-toepassing herstelt de koolstof in de bodem en de productiviteit
Char-toepassing herstelt de koolstof in de bodem en de productiviteit Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen
Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River
Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River Ongekende overstromingen in het noordoosten van Australië
Ongekende overstromingen in het noordoosten van Australië
Hoofdlijnen
- Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
- P53 (TP53) Tumor Protein: Function, Mutation
- Dierlijke versus plantencellen: overeenkomsten en verschillen (met grafiek)
- Analyse van oud DNA onthult een voorheen niet-herkend geslacht van uitgestorven paarden dat ooit door Noord-Amerika zwierf
- Australische soorten hebben een onafhankelijke kampioen nodig
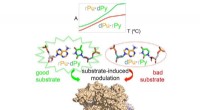
- Onderzoekers ontdekken moleculaire add-ons die eiwitinterfaces aanpassen
- Onderzoekers ontdekken hoe cellen decennia later infecties onthouden
- Stamcellen die vetweefsel genereren, hebben een circadiane klok
- Uitbreiding van Braziliaans suikerriet kan de wereldwijde CO2-uitstoot verminderen
- Wetenschappers ontdekken nieuw bacterieel resistentiemechanisme tegen peptide-antibiotica
- Draagbare biosensor waarschuwt voor hartaanval en beroerte

- Hoe de grootte van een Atom

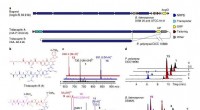
- Onderzoekers identificeren de bron van asymmetrie in RNA-DNA-hybriden
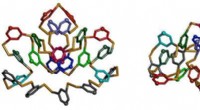
- Zelfgebouwde gevouwen macrocycles maken met lage symmetrie
 Het gebruik van mobiele apparaten thuis kan conflicten naar de werkplek brengen
Het gebruik van mobiele apparaten thuis kan conflicten naar de werkplek brengen Brexit 1.0:wetenschappers vinden bewijs van de oorspronkelijke scheiding van Groot-Brittannië van Europa
Brexit 1.0:wetenschappers vinden bewijs van de oorspronkelijke scheiding van Groot-Brittannië van Europa Cop stem:Jay-Z, Public Enemy-liedjes benadrukken politietactieken om mensen van kleur bang te maken
Cop stem:Jay-Z, Public Enemy-liedjes benadrukken politietactieken om mensen van kleur bang te maken Displays maken met rijkere kleuren
Displays maken met rijkere kleuren Hoe driehoekshoekmetingen te vinden
Hoe driehoekshoekmetingen te vinden Kunnen ethieklessen het moreel gedrag van studenten daadwerkelijk beïnvloeden?
Kunnen ethieklessen het moreel gedrag van studenten daadwerkelijk beïnvloeden? Hoog boven de Groenlandse gletsjers, NASA onderzoekt smeltend oceaanijs
Hoog boven de Groenlandse gletsjers, NASA onderzoekt smeltend oceaanijs Ryanair-voorzitter krijgt klap van aandeelhouder te midden van stakingen
Ryanair-voorzitter krijgt klap van aandeelhouder te midden van stakingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

